一、PD-1/PD-L1靶点概述
● PD-1/PD-L1的结构与表达
①PD-1:PD-1,又名CD279,属于CD28超家族,由位于人类2号染色体的PDCD1基因编码。其蛋白其蛋白是I型膜蛋白,胞外IgV型结构域、20个氨基酸的柄部、跨膜结构域以及含免疫受体酪氨酸抑制基序(ITIM)和免疫受体酪氨酸转换基序(ITSM)的胞内结构域。PD-1与配体结合后,招募SHP-2磷酸酶,影响TCR信号通路,抑制T细胞活化。
②PD-L1:PD-L1,也叫CD274或B7-H1,属于B7家族,由人类9号染色体上的CD277基因编码。是一种I型跨膜蛋白,包含IgV样和IgC样胞外结构域、疏水跨膜结构域及含30个氨基酸的短胞质尾。在肿瘤环境中,PD-L1作为促肿瘤因子,能增加肿瘤细胞的增殖和存活信号通路。
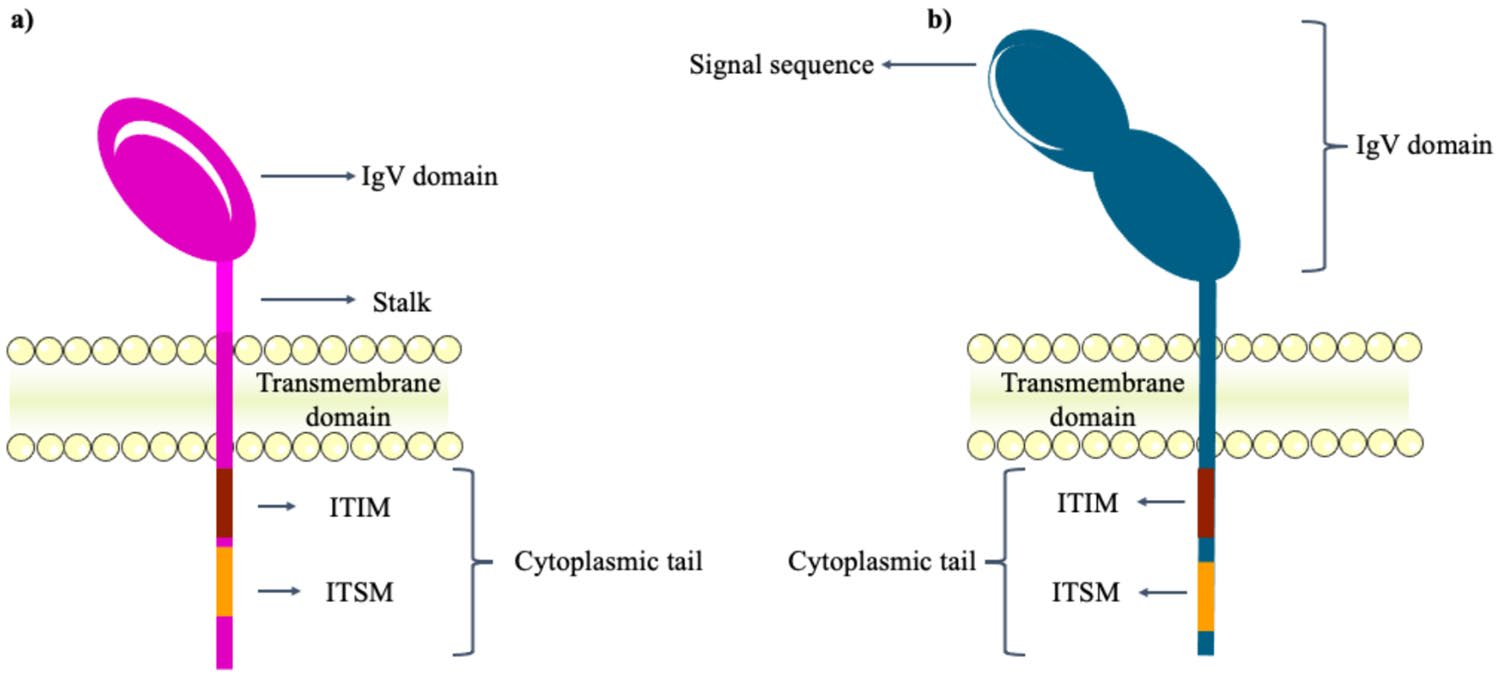
图1 PD-1和PD-L1的结构示意图
● PD-1/PD-L1在不同免疫细胞中的作用
①T细胞:影响T细胞激活、耐受和耗竭,其异常表达破坏免疫平衡。在肿瘤微环境中,PD-1上调助力肿瘤免疫逃逸。
②B细胞:调节B细胞激活、增殖和免疫耐受。在类风湿关节炎、肿瘤和乙肝等疾病中,PD-1参与B细胞功能失调,阻断PD-1可恢复部分B细胞功能。
③其他细胞:在树突状细胞(DCs)、自然杀伤细胞(NK细胞)、巨噬细胞、固有淋巴细胞(ILCs)、单核细胞和中性粒细胞中均有表达,且在不同疾病状态下对细胞功能产生不同影响,如抑制DCs的抗原呈递能力、改变NK细胞的抗肿瘤功能等。
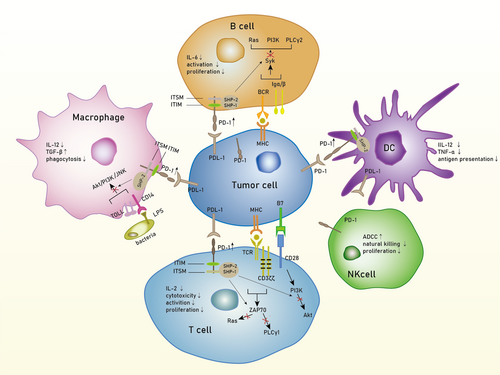
图2 PD-1在T细胞、B细胞、NK细胞、DC和巨噬细胞上的表达上调
● PD-1/PD-L1与配体的相互作用
PD-1/PD-L1轴是免疫系统中的关键信号通路。PD-1作为一种重要的免疫抑制分子,广泛表达于T细胞、B细胞、NK细胞等多种免疫细胞表面,在维持免疫耐受方面发挥着关键作用,保护正常组织免受免疫攻击,同时与多种疾病的免疫失调相关。其配体PD-L1则由肿瘤微环境中癌细胞和抗原呈递细胞产生。二者结合会干扰T细胞受体的信号转导,抑制T细胞的生存、增殖和活性,从而削弱抗癌免疫,助力肿瘤细胞逃避机体免疫系统的监视和攻击,阻碍抗癌免疫反应。在炎症性疾病中,其表达异常可加剧或促进炎症;在感染过程中,其表达变化有助于区分急慢性感染。此外,PD-1与PD-L1的相互作用可发生在反式和顺式构型。反式作用抑制T细胞反应,而顺式作用会降低经典的PD-L1/PD-1抑制信号。
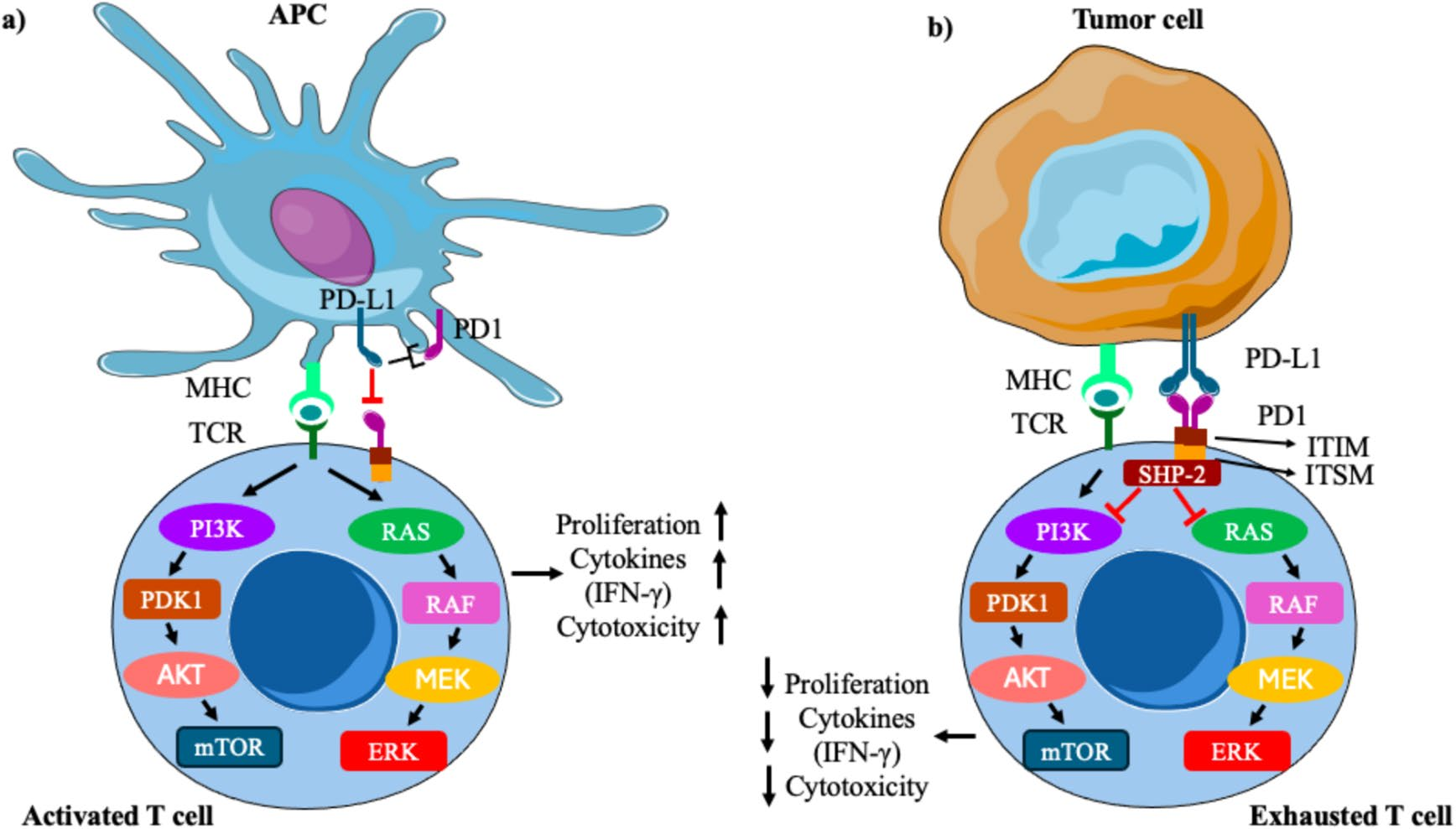
图3 PD-1/PD-L1之间的相互作用
● PD-1/PD-L1的生理功能
在正常生理条件下,PD-1与PD-L1是维持免疫稳态的重要分子,它们的结合能抑制T细胞的激活来维持免疫平衡,减少自身免疫细胞对自身组织的攻击,防止组织炎症和自身免疫疾病的发生。当细胞癌变时,癌细胞会利用这一抑制途径逃避免疫系统的攻击。此外,PD-1/PD-L1还通过激活SHP2抑制T细胞信号传导,减弱免疫应答,在细胞黏附、迁移、记忆T细胞形成及代谢等方面发挥重要作用,还参与组织和器官的发育、再生等过程。
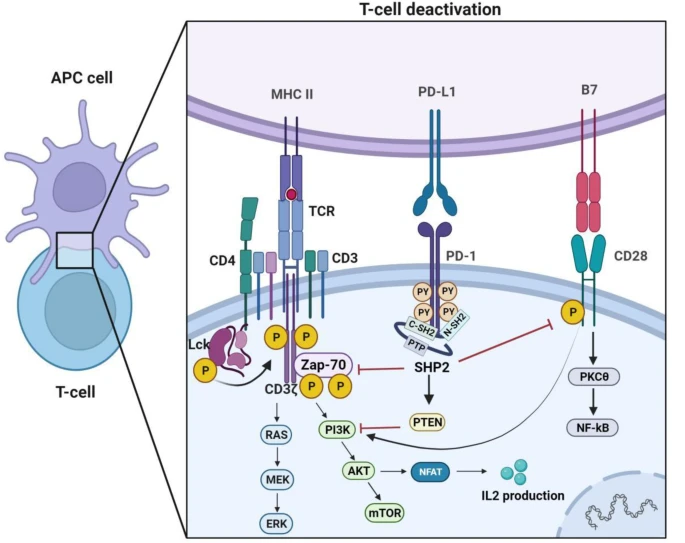
图4 PD-1/PD-L1轴的免疫调节机制
研究还发现该通路在多种疼痛模型中作用关键,其激活能调节巨噬细胞、小胶质细胞、T细胞的增殖、活化与极化,抑制伤害感受神经元兴奋性,减轻炎症反应和疼痛。
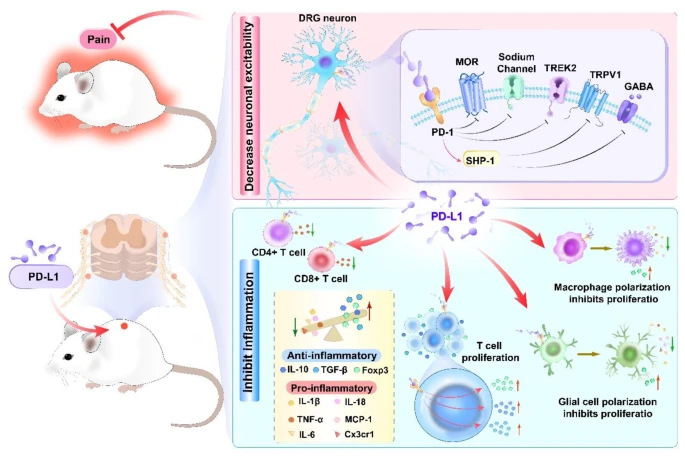
图5 PD-L1/PD-1通路在疼痛中的机制概述
二、PD-1/PD-L1表达的调控机制
● PD-1/PD-L1的表达调控
①PD-1:PD-1表达受多种因素影响,如抗原信号刺激、炎症因子等。在急性感染和慢性感染中,PD-1表达的调控机制不同。在肿瘤免疫中,持续的TCR信号可导致PD-1表达增加,诱导免疫耐受。
②PD-L1:PD-L1表达受基因水平(如基因扩增、结构变异等)、表观基因组水平(DNA甲基化、组蛋白修饰等)、转录和转录后水平(转录因子、非编码RNA、RNA甲基化等)以及翻译后修饰水平(糖基化、磷酸化、泛素化等)的调控,同时肿瘤微环境也可影响PD-L1表达。
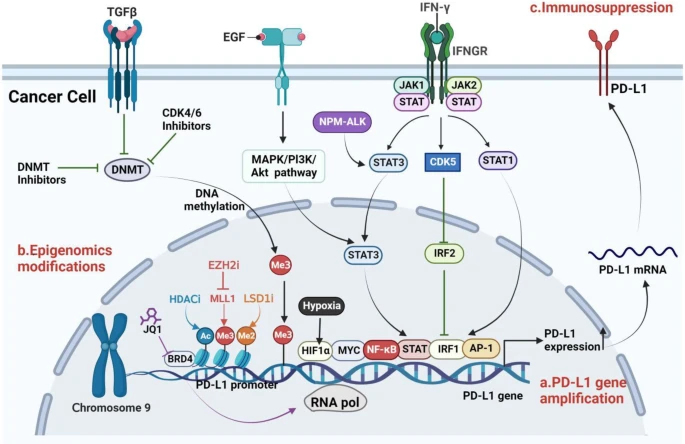
图6 PD-L1表达的遗传和转录调控机制
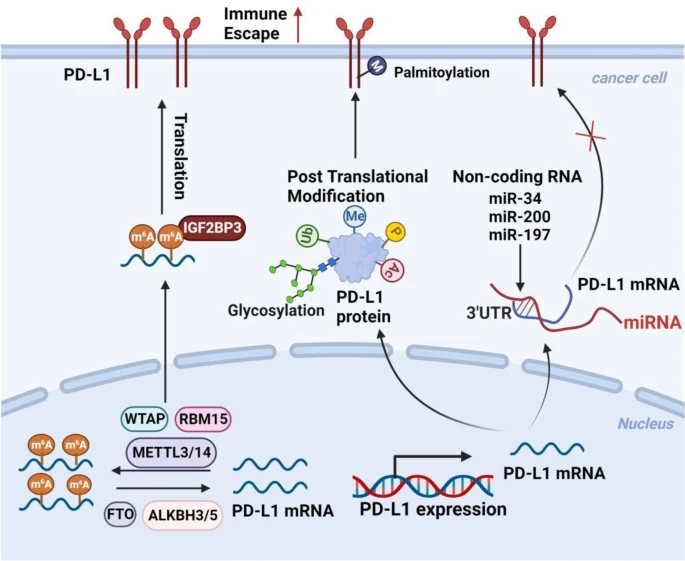
图7 PD-L1转录后和翻译后表达调节机制
● 相关信号通路
PD-1/PD-L1轴在肿瘤微环境中,通过多种信号通路促进肿瘤进展和逃逸。激活PI3K/AKT、MAPK、JAK-STAT等通路,影响细胞增殖、存活和免疫逃逸;还涉及Wnt、NF-κB、Hh等通路,在肿瘤发展各阶段发挥关键作用。
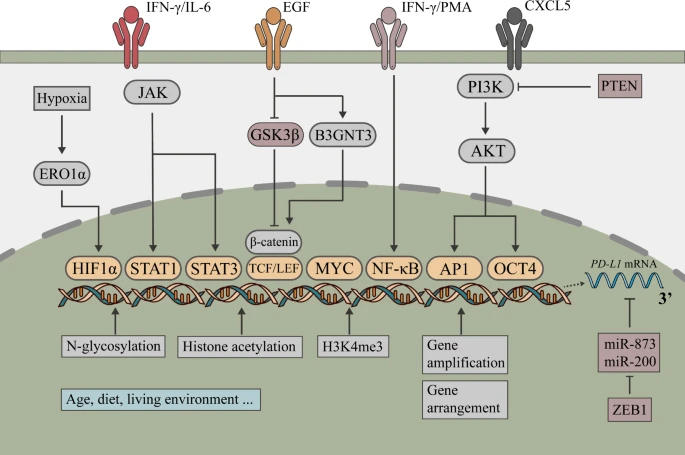
图8 PD-L1表达调控的相关信号通路

表1 PD-1/PD-L1参与的相关信号通路
三、PD-1/PD-L1的病理功能
● PD-1/PD-L1在移植和自身免疫疾病中的作用
①移植:PD-1/PD-L1信号可抑制移植后T细胞的活化和增殖,减轻免疫排斥。但在部分癌症患者接受免疫治疗时,可能引发免疫相关不良反应,影响预后,临床应用免疫治疗时,需谨慎评估风险并选择合适的治疗方案。
②自身免疫疾病:PD-1/PD-L1与多种自身免疫疾病相关,如1型糖尿病、系统性红斑狼疮、多发性硬化症和类风湿关节炎等,其平衡被打破,影响疾病进程。PD-1/PD-L1在疾病发生发展中起复杂作用,阻断PD-1/PD-L1可能加重病情。针对其的治疗研究正在不断探索,如靶向PD-1的免疫毒素可改善自身免疫疾病。
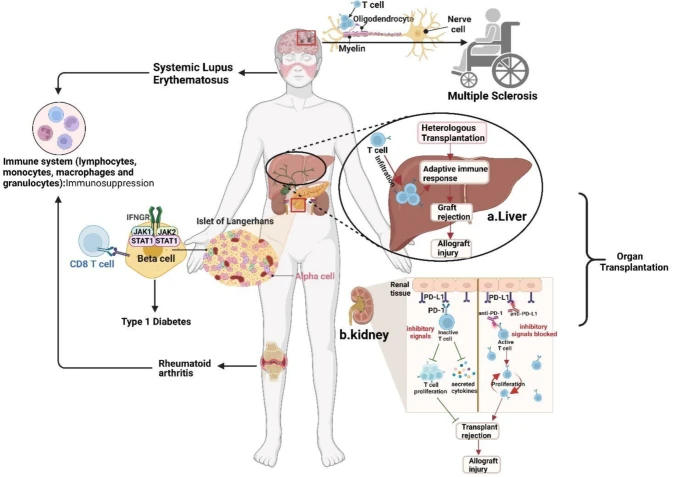
图9 PD-1/PD-L1在移植和自身免疫性疾病中的作用
● PD-1/PD-L1在肿瘤中的作用
①促进肿瘤发生发展:肿瘤细胞常高表达PD-L1,其与T细胞表面的PD-1结合,抑制T细胞的活化、增殖和细胞因子分泌,使T细胞功能障碍、失活和耗竭,无法有效识别和杀伤肿瘤细胞,帮助肿瘤细胞逃避免疫系统的监测和攻击。此外,PD-1/PD-L1轴还可抑制NK细胞的脱颗粒和细胞毒性功能,降低其杀死肿瘤细胞的能力,进一步促进肿瘤免疫逃逸。
②调节肿瘤微环境:肿瘤微环境(TME)在癌症发展中起重要作用,免疫细胞的组成和相互作用影响肿瘤的进展和免疫反应。PD-1/PD-L1相互作用会诱导肿瘤相关巨噬细胞(TAM)向M2表型极化,使其释放大量成纤维细胞生长因子、VEGF、TNF-α等细胞因子,这些因子可促进血管生成,为肿瘤细胞提供营养和转移途径;还能营造免疫抑制环境,支持肿瘤细胞的侵袭和转移,加速癌症进展。同时,PD-1/PD-L1轴的激活可促进调节性T细胞(Tregs)的产生和发育,增强其免疫抑制功能,诱导免疫耐受,有利于肿瘤细胞在体内存活和增殖。
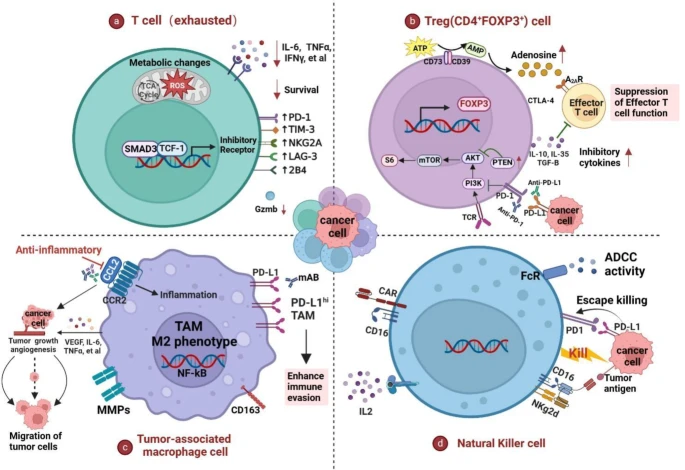
图10 PD-1/PD-L1信号对免疫细胞的调节
③肿瘤细胞代谢与增殖调控:PD-1/PD-L1信号可改变细胞能量合成和代谢途径,破坏有氧糖酵解,促使脂肪酸氧化成为T细胞的主要能量来源,影响免疫细胞功能的同时,也为肿瘤细胞的生长和增殖创造有利条件。
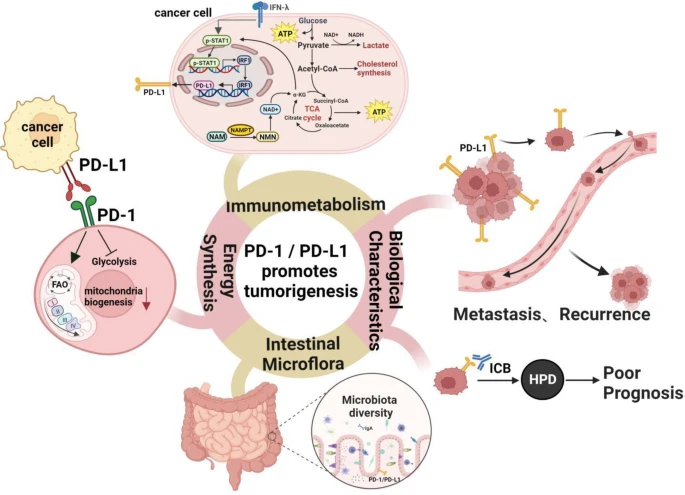
图11 PD-1/PD-L1信号传导影响细胞能量合成和代谢
④影响肿瘤复发和预后:PD-1/PD-L1参与肿瘤的转移和复发,其高表达与肿瘤预后相关。高表达PD-L1的肿瘤患者对PD-1/PD-L1抑制剂更敏感,但部分患者可能出现超进展疾病,需要探索预测生物标志物以优化治疗。
⑤肿瘤细胞内的非免疫功能:PD-L1在肿瘤细胞内存在多种形式,核PD-L1可参与肿瘤细胞的多种生物学过程,如调节基因组稳定性、促进肿瘤细胞增殖等;肿瘤细胞内的PD-1也具有复杂的作用,可能抑制或促进肿瘤生长,取决于肿瘤类型和信号通路。
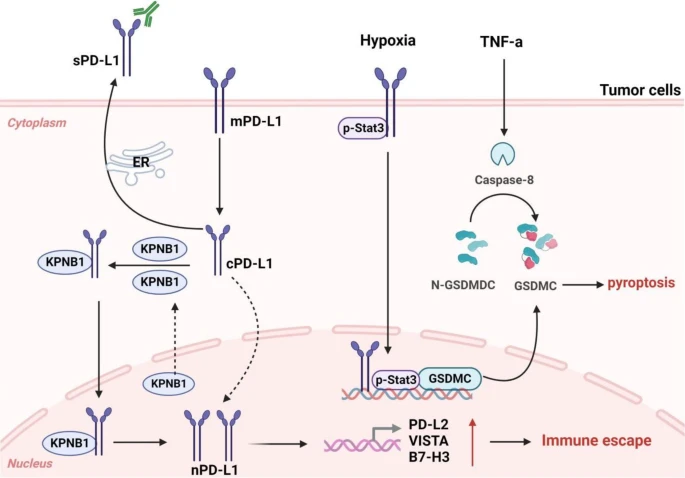
图12 核PD-L1对肿瘤本身的影响
四、PD-1/PD-L1的免疫治疗
● PD-1/PD-L1在肿瘤免疫治疗中的应用
①作为癌症生物标志物:检测肿瘤细胞或免疫细胞的PD-1/PD-L1表达,可预测患者对免疫治疗的反应,但存在局限性,不同肿瘤类型中其预测意义不同,检测结果的可重复性和准确性有待提高。
②评估预后:可溶性PD-L1(sPD-L1)具有预后价值,治疗前sPD-L1水平高与预后不良相关;治疗后sPD-L1水平快速升高,提示肿瘤特异性免疫反应强烈,与较高的部分缓解率相关。
● 治疗方法
目前针对PD-1/PD-L1的肿瘤免疫治疗方法包括使用免疫检查点抑制剂、过继性T细胞疗法、基因编辑疗法和肿瘤疫苗等。其中基于PD-1/PD-L1的肿瘤免疫治疗药物主要包括免疫检查点抑制剂,如已获批的多种PD-1抑制剂(如pembrolizumab、nivolumab、cemiplimab等)和PD-L1抑制剂(如atezolizumab、avelumab、durvalumab等)。这些药物已广泛应用于黑色素瘤、非小细胞肺癌、头颈部癌等多种癌症的治疗,显著提高了部分患者的总体生存率和无进展生存率,但仍存在低响应率和耐药性等局限性。
● 药物类型
目前有13种抗PD-1单克隆抗体上市,涵盖18种癌症类型,还有2081项PD-1相关临床试验正在进行。新型抗体如anti-c-Met/PD-1双抗体等处于临床试验阶段,同时也在开发小分子抑制剂、环肽抑制剂等新型PD-1抑制剂。大量临床试验从总生存期(OS)、客观缓解率(ORR)和无进展生存期(PFS)等方面评估了PD-1/PD-L1免疫检查点抑制剂的疗效,发现同一抑制剂对不同癌症的治疗效果存在差异。
①靶向PD-1/PD-L1的mAbs:阻断PD-1/PD-L1通路能增强抗肿瘤T细胞活性,引发内源性免疫反应。目前获批用于临床的主要是mAbs,多种PD-1/PD-L1阻断mAbs已获批用于癌症免疫治疗,对多种癌症有效。然而,mAbs存在患者响应率低、易复发、肿瘤穿透性差、成本高和免疫相关副作用等问题,促使研究人员开发新型免疫治疗药物,如SMIs。
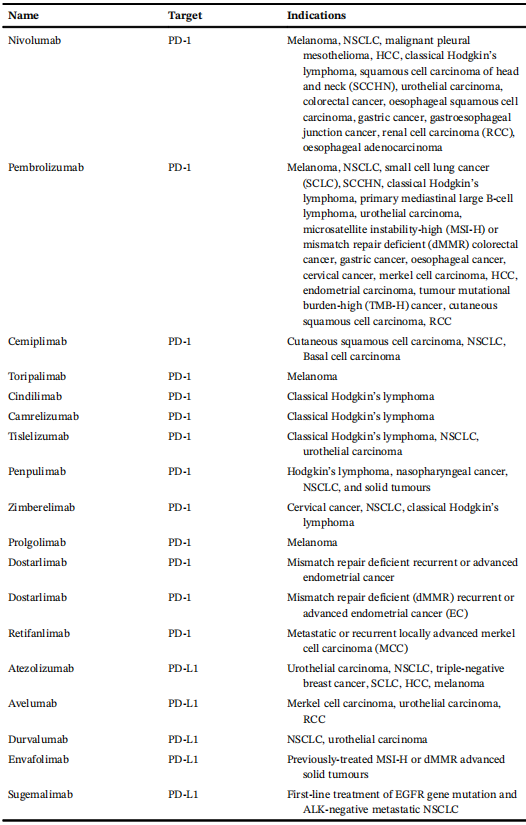
表2 已上市的靶向PD-1/PD-L1的单克隆抗体
②靶向PD-1/PD-L1轴的小分子抑制剂(SMIs):近年来众多靶向PD-L1的SMIs被研发,部分已进入临床试验。这些SMIs通过不同机制抑制PD-1/PD-L1相互作用,展现出良好的抗肿瘤潜力。SMIs具有半衰期短、成本低、稳定性好、肿瘤穿透性强等优势,但目前其发展受限于蛋白质结合结构信息不足。BMS开发的非肽类小分子能抑制PD-1/PD-L1相互作用,为新药开发提供了起点。
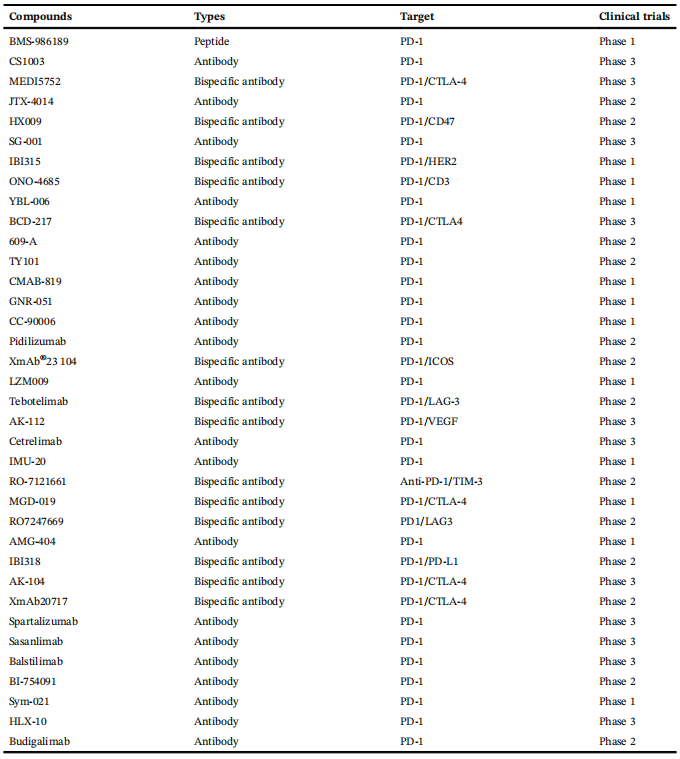
表3 临床试验中靶向PD-1的化合物
③靶向PD-1/PD-L1的BsAbs:多种靶向PD-1/PD-L1的BsAb在临床前和临床试验中展现出抗肿瘤活性。例如,抗TGFβ×PD-L1的M7824、抗CD47×PD-L1的6MW3211、抗VEGF×PD-1的AK112等。这些BsAb通过阻断相关信号通路,增强免疫细胞功能,抑制肿瘤生长和转移,部分已进入后期临床试验阶段,为癌症治疗提供了新选择。
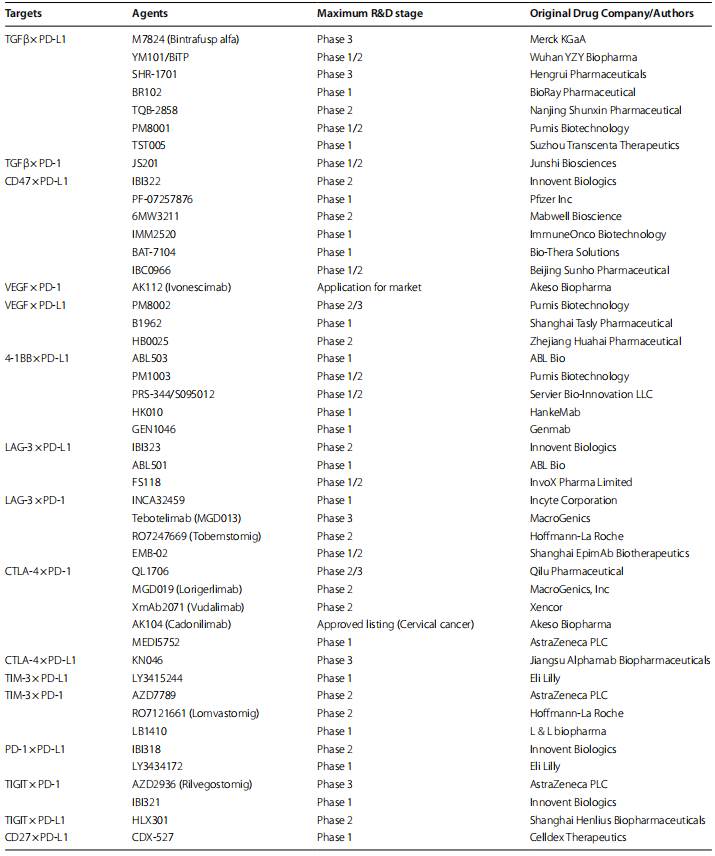
表4 靶向PD-1/PD-L1信号的双特异性/双功能抗体的研究进展
④靶向PD-1/PD-L1的PROTACs:靶向PD-1/PD-L1的PROTACs是一种新型癌症免疫治疗策略,它由靶蛋白配体、E3泛素配体和连接子组成,通过招募E3泛素连接酶使PD-1或PD-L1蛋白泛素化并被蛋白酶体降解,从而阻断肿瘤免疫逃逸通路。目前已开发出如Compound22、AC-1、CDTACs等多种PROTACs,在临床前研究中展现出对PD-1/PD-L1的有效降解和良好的抗肿瘤活性,部分已进入临床试验探索阶段,但仍面临膜蛋白靶向降解、分子设计优化、脱靶效应和免疫相关不良反应等挑战,未来有望通过技术创新和联合治疗进一步提高癌症治疗效果。
● 联合治疗策略
①与其他免疫检查点抑制剂联合:PD-1/PD-L1抑制剂与CTLA-4抑制剂联合治疗,在多种癌症中显示出更强的抗肿瘤活性,可提高患者的生存率。此外,PD-1/PD-L1抑制剂还可与TIM-3、TIGIT、LAG-3等免疫检查点抑制剂联合,目前部分联合方案正在临床试验阶段。
②与靶向药物联合:包括与抗血管生成药物、EGFR-TKIs、PARP激酶抑制剂等联合。抗血管生成药物与PD-1/PD-L1抑制剂联合,可通过调节肿瘤血管,增强免疫细胞浸润,提高治疗效果。
③与放疗和化疗联合:放疗可将肿瘤转化为原位疫苗,激活全身免疫反应,与PD-1/PD-L1抑制剂联合能增强抗肿瘤免疫。化疗则可促进T细胞浸润肿瘤组织,降低免疫抑制细胞数量,与PD-1/PD-L1抑制剂联合可提高治疗效果。但化疗存在骨髓抑制等严重副作用,需要谨慎选择方案并密切监测。
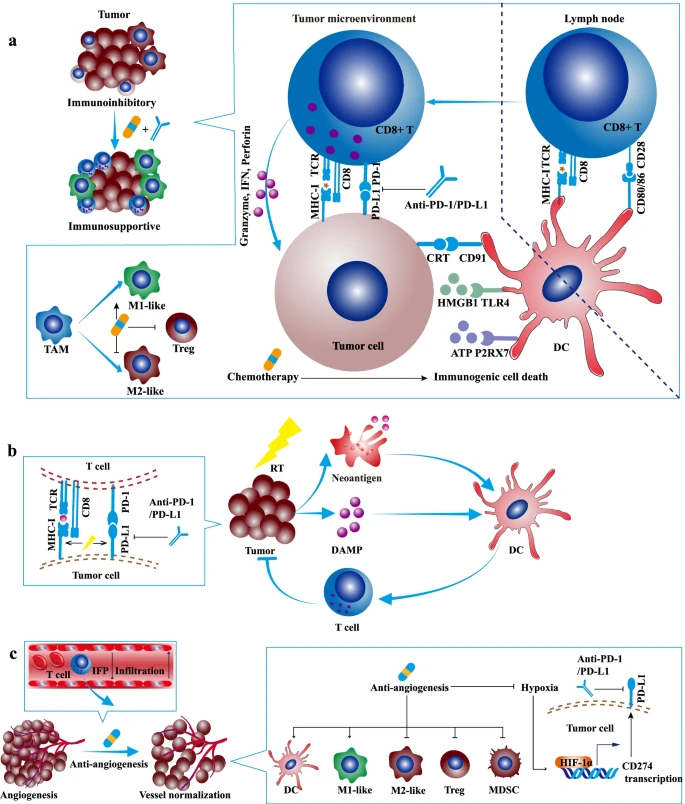
图13 PD-1/PD-L1联合化疗、放疗或血管生成抑制剂的协同抗肿瘤疗效和机制
④与其他疗法联合:如与血管生成抑制剂、CAR-T细胞疗法、光动力疗法、适配体药物结合物、溶瘤病毒疗法、癌症疫苗等联合。这些联合治疗方案在临床前研究或临床试验中展现出一定的潜力,为肿瘤治疗提供了更多选择。
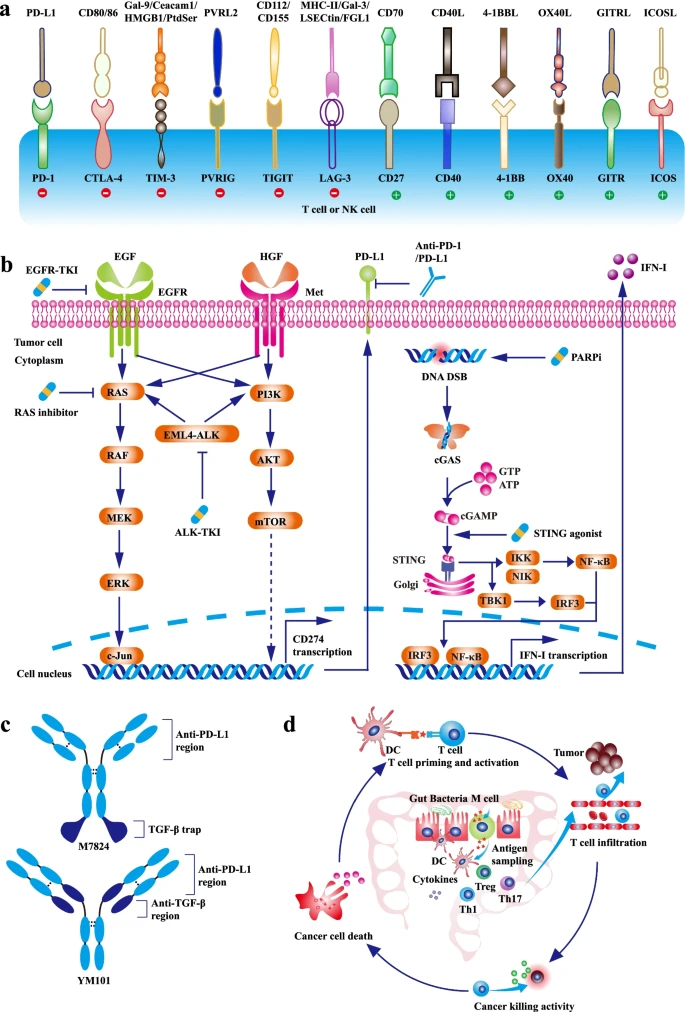
图14 PD-1/PD-L1与其他新疗法联合使用的协同抗肿瘤疗效和机制
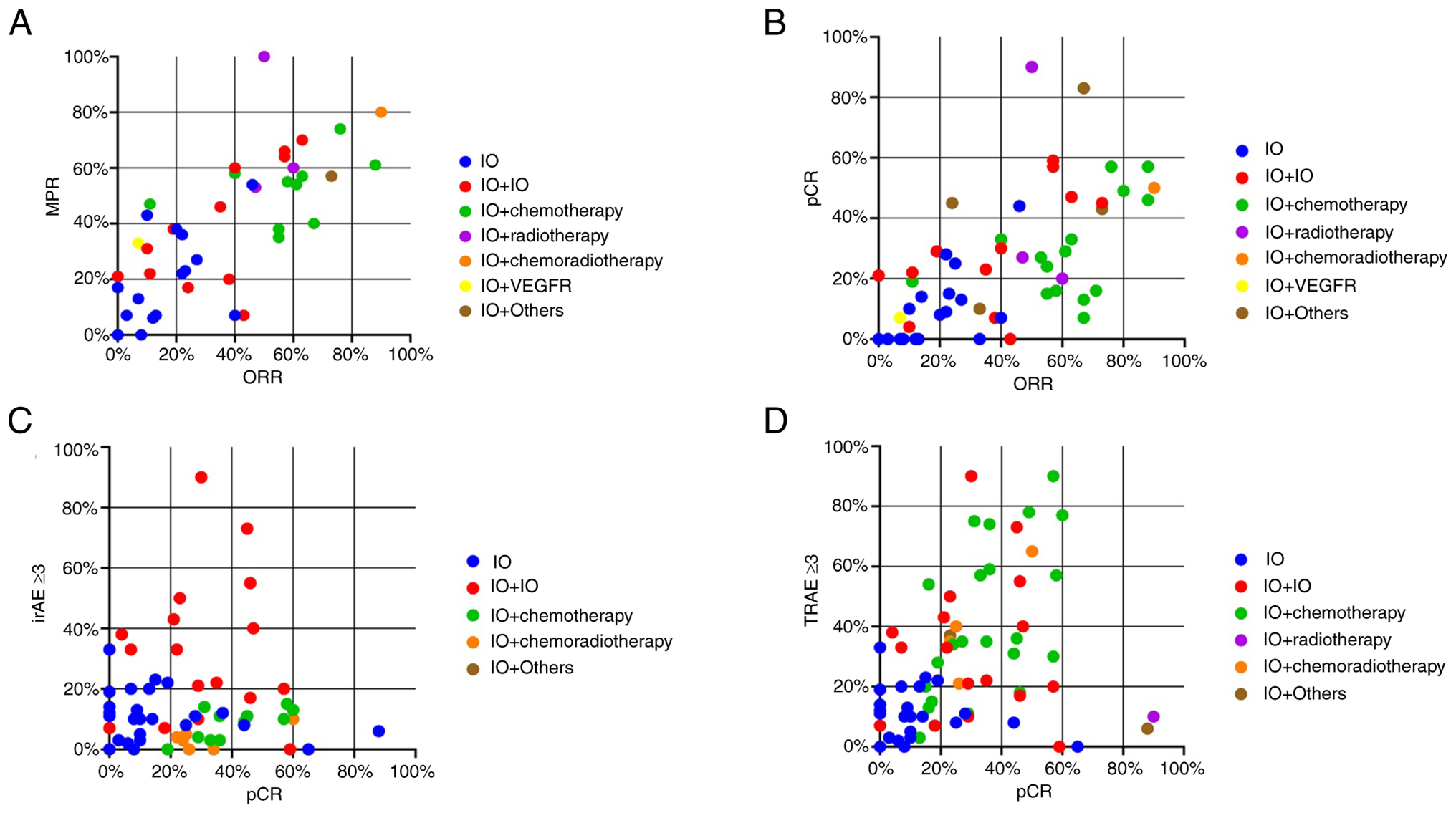
图15 PD-1/PD-L1联合治疗的ORR、MPR、pCR和AE(包括TRAEs和irAEs)
● PD-1/PD-L1介导的免疫耐药和副作用
肿瘤细胞对PD-1/PD-L1单抗产生耐药的原因较为复杂,包括肿瘤细胞内在的免疫逃逸遗传途径、肿瘤抗原突变和呈递过程异常、多个免疫检查点之间的相互作用、抑制性肿瘤微环境、致癌途径激活、关键肿瘤蛋白的表观遗传变化以及代谢产物积累等。分为原发性耐药和获得性耐药。原发性耐药机制包括肿瘤免疫原性缺乏、T细胞排除等;获得性耐药与T细胞功能耗竭、新抗原处理或呈递受损等因素有关。PD-1/PD-L1免疫检查点抑制剂治疗癌症会引发免疫相关不良事件(irAEs),如内分泌毒性、肝毒性、皮疹、甲状腺功能减退等,且具有持续时间长、发病延迟的特点,需要加强管理和治疗。
五、PD-1/PD-L1在多种癌症中的应用
● 实体瘤
①肺癌:免疫检查点抑制剂改善晚期患者预后,PD-L1高表达与更高疗效相关,还可检测血液中PD-1和PD-L1用于辅助指导治疗。但部分患者会出现超进展疾病(HPD),联合治疗成为重要策略。
②乳腺癌:免疫疗法在乳腺癌中应用较少,转移性三阴性乳腺癌对PD-1/PD-L1抑制剂有潜在反应,且PD-L1表达与高风险临床病理参数和不良预后相关,联合化疗可能是新的临床范式。
③胃癌:PD-1靶向治疗对转移性胃癌患者有效,疗效与PD-L1表达相关,且自噬可能与抗PD-1/PD-L1免疫治疗相关。但单药治疗效果存在争议,需进一步临床试验确认。
④血管肉瘤:免疫治疗成为治疗血管肉瘤的热点,PD-L1在约66%的样本中异常表达,对部分患者疗效显著。高PD-L1表达与其疾病的进展相关,联合免疫检查点抑制剂和aPKC抑制剂可能是潜在治疗策略。
⑤前列腺癌:PD-1/PD-L1免疫检查点抑制剂虽给部分患者带来临床获益,但因肿瘤免疫原性低,总体效果不佳。高PD-1+淋巴细胞密度与临床失败相关,联合放疗等可能是有前景的策略。
⑥结直肠癌:对dMMR或MSI-H的转移性结直肠癌患者疗效较好,对pMMR或MSS肿瘤患者疗效不佳。联合治疗为难治性或转移性结直肠癌的治疗带来希望。
⑦肝癌:PD-1/PD-L1表达与肿瘤免疫和预后相关,免疫检查点抑制剂治疗可改善患者总生存期,联合治疗是有效策略。目前缺乏综合预测生物标志物。
⑧膀胱癌:免疫治疗已获批准,PD-1和PD-L1的表达与膀胱癌的病理分级和进展相关。PD-1/PD-L1免疫检查点抑制剂联合自噬抑制剂或放疗可能是有前景的治疗方法。
⑨卵巢癌:应用PD-1/PD-L1抑制剂治疗引起广泛关注,单药治疗效果不佳,联合治疗可能是有效策略。临床实践中存在剂量、亚型反应差异和副作用等问题。
⑩胰腺癌:PD-L1是预后新标志物,PD-1/PD-L1表达与肿瘤进展相关。单药治疗效果不理想,联合治疗策略可能带来新希望。
● 血液瘤
①多发性骨髓瘤:PD-1/PD-L1相互作用抑制免疫功能,促进肿瘤免疫逃逸。单药治疗效果不乐观,联合治疗展现出潜力,但结论不一致,需更多研究。
②白血病:高表达PD-1和PD-L1与患者较差的总生存期和临床结果相关,联合治疗显示出一定前景,但临床反应存在差异,仍需进一步研究。
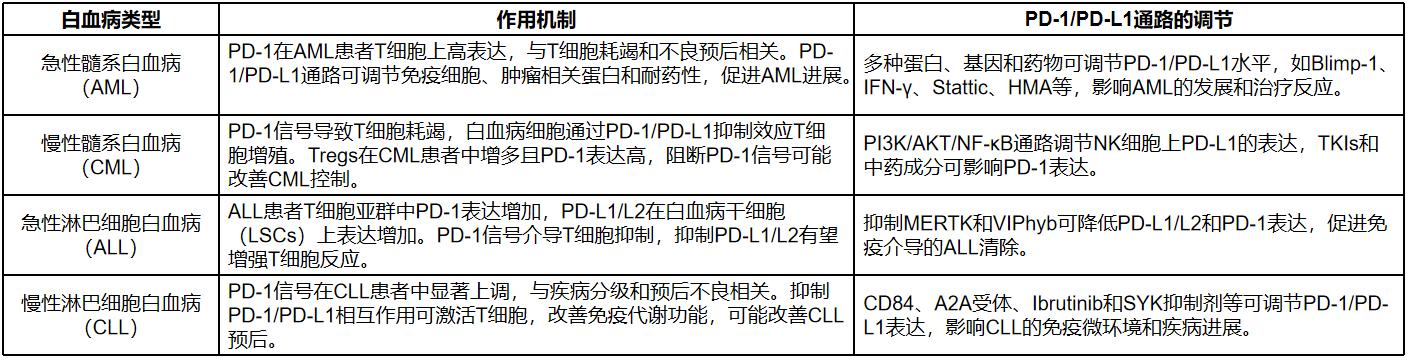
表5 PD-1/PD-L1在在不同类型白血病中的治疗潜力
③淋巴瘤:PD-1/PD-L1抑制剂在淋巴瘤治疗中取得一定成果,但在不同亚型中的表达水平和作用存在差异,需要更精确和个体化的临床试验。
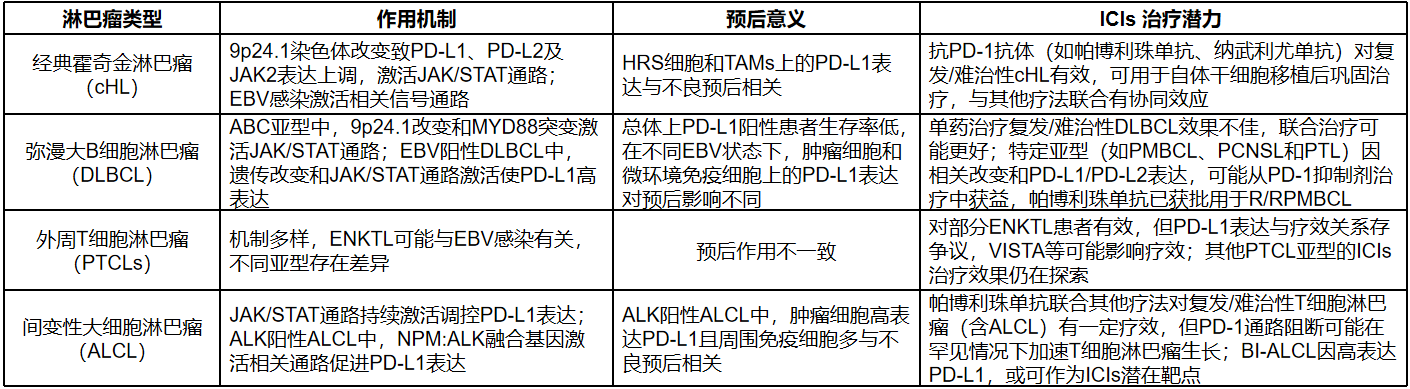
表6 PD-1/PD-L1在在不同类型淋巴瘤中的治疗潜力