一、LAG3的基本结构与功能
● LAG3的全称与别名:Lymphocyte activation gene3(LAG-3),又称CD223,是一种新兴的免疫检查点分子,与PD-1、CTLA-4同属免疫抑制性受体。
● LAG3的分子结构:LAG3是一种17:33:53Ⅰ型跨膜蛋白,属于免疫球蛋白超家族,与CD4结构相似,其结构包括4个Ig样胞外结构域(D1-D4)、跨膜区和胞内结构域(包含FxxL、KIEELE和EP等抑制性基序),需同源二聚化发挥功能。
● LAG3的同源二聚化:D2结构域的疏水残基(如Trp180、Leu221)介导二聚化,是配体结合和信号传导的必要条件。靶向D2结构域的抗体(如C9B7W)可阻断二聚化,增强抗肿瘤免疫。
● LAG3的配体结合:配体通过结合LAG3的D1结构域调节T细胞功能。主要配体包括:
①FGL1(纤维蛋白原样蛋白1):主要免疫抑制配体,是肝脏分泌的可溶性蛋白,与LAG-3高亲和力结合,干扰TCR-CD3复合体近端信号传导,降低T细胞增殖和细胞毒性(如IFN-γ、穿孔素分泌减少)。在多种癌症中高表达,与肝癌、胃癌的不良预后、免疫治疗耐药相关,阻断FGL1-LAG3轴可增强抗肿瘤免疫。纳米抗体和TR-FRET技术用于高灵敏度检测FGL1/LAG-3相互作用,助力药物筛选。可溶性FGL1蛋白或抗体可作为潜在治疗工具,调节T细胞功能。
②MHCⅡ类分子(pMHCⅡ):经典配体,亲和力强,选择性结合稳定的肽-MHCII复合物(pMHCII),优先抑制识别该复合物的T细胞,阻断TCR信号传导并激活肿瘤细胞生存通路(如MAPK/Erk、PI3K/Akt),增强肿瘤细胞抗凋亡能力并促进肿瘤免疫逃逸。
③TCR-CD3复合体:在无MHCII时结合,可作为顺式配体,通过EP基序降低免疫突触pH值,干扰酪氨酸激酶Lck与共受体结合,抑制T细胞活化。
④LSECtin(肝窦内皮细胞凝集素)/Galectin-3(半乳凝素-3):参与肿瘤微环境免疫逃逸,如黑色素瘤细胞表达,LSECtin抑制效应T细胞增殖及IFN-γ分泌,促进肿瘤生长,但在其他肿瘤中作用有限。Galectin-3通过糖基化结合LAG-3,抑制CD8+T细胞增殖和APC功能,在子宫内膜癌、多发性骨髓瘤等肿瘤中参与免疫抑制。
⑤α-突触核蛋白(α-syn):神经元中LAG-3配体,促进α-syn纤维传递,与帕金森病发病相关,抗LAG-3抗体可阻断这一过程。
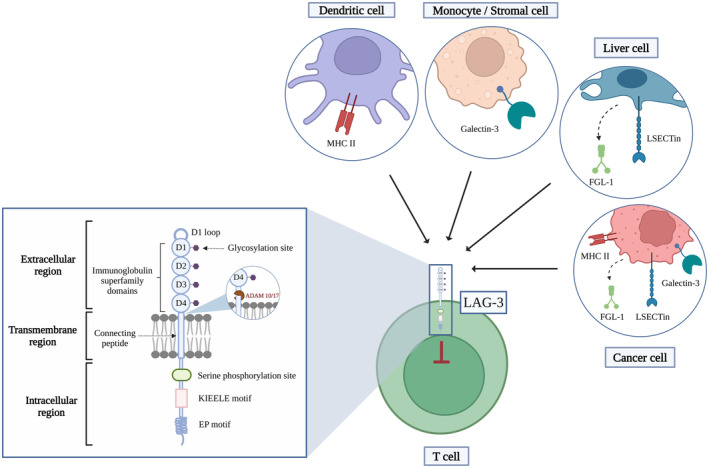
图1 LAG-3的结构及其与配体的相互作用
● LAG3的功能机制:LAG3与PD-1、TIM3、CTLA-4等抑制分子共表达于耗竭T细胞(TEX)表面,形成“免疫检查点网络”,协同抑制抗肿瘤免疫。共靶向多个抑制性受体(IRs)成为治疗策略之一。、
● 可溶性LAG3(sLAG3):胞外域被ADAM10/17蛋白酶剪切后产生可溶性sLAG3,其高水平与黑色素瘤和头颈部鳞癌等部分癌症预后不良相关,但其功能仍不明确。血清中sLAG3水平可能作为预测免疫治疗反应的生物标志物。
二、LAG3的表达调控与功能机制
● LAG3的细胞分布与组织定位
①免疫细胞:初始T细胞低表达,激活后显著上调,富集于耗竭T细胞和调节性T细胞(Tregs)。广泛表达于B细胞、NK细胞、浆细胞样树突状细胞(pDCs)及非免疫细胞(如神经元)表面。在肿瘤浸润T细胞(TILs)中高表达,是T细胞耗竭的标志性分子之一。
②肿瘤细胞:在结直肠癌、乳腺癌、黑色素瘤、非小细胞肺癌(NSCLC)、卵巢癌等实体瘤的肿瘤细胞中异常表达,其水平与肿瘤分期(如TNM分期)、转移能力、生存期和预后正相关。
● LAG3的调控机制
①转录调控:IL-6通过激活STAT3通路直接诱导LAG3在CD8⁺T细胞中表达,外周血中IL-6水平、CD8⁺T细胞LAG3表达可作为预测LAG3阻断疗效的生物标志物。此外,FSTL1(卵泡抑素样蛋白1)也参与LAG3的调控,通过诱导CD11b⁺DIP2A⁺LAG3⁺细胞生成,促进结直肠癌免疫逃逸,形成“FSTL1-LAG3轴”。
②表观遗传:LAG3甲基化状态与结直肠癌肿瘤风险呈负相关,但其甲基化状态在不同瘤种中稳定性不足,需更大样本验证。此外,LAG3的表观修饰还调控免疫检查点共表达,如PD-L1与LAG3的共甲基化影响免疫治疗响应。
● LAG-3在免疫细胞中的功能
①T细胞:LAG-3通过结合配体抑制CD4+/CD8+T细胞的增殖、细胞因子分泌(如IL-2、IFN-γ、TNF-α)及细胞毒性,导致T细胞耗竭。在肿瘤微环境(TME)中,LAG-3+肿瘤浸润淋巴细胞(TILs)表现出功能失调,与不良预后相关。调节性T细胞(Tregs):Tregs表面LAG-3表达上调可增强其免疫抑制能力,通过抑制效应T细胞和促进APC功能失活维持免疫耐受。LAG-3缺陷会削弱Tregs的抑制功能,加剧自身免疫反应。
②NK细胞与其他免疫细胞:LAG-3抑制NK细胞的细胞毒性和细胞因子生成,但单独阻断对NK细胞毒性影响有限,联合IL-12可恢复其抗转移活性。膜结合LAG-3与树突状细胞(DCs)表面MHCII结合,促进DCs成熟,分泌IL-12和TNF-α;但可溶性LAG-3抑制单核细胞向DCs分化,削弱免疫应答。浆细胞样树突状细胞(pDCs)中LAG-3LAG-3抑制pDCs产生I型干扰素,影响抗病毒和抗肿瘤免疫。
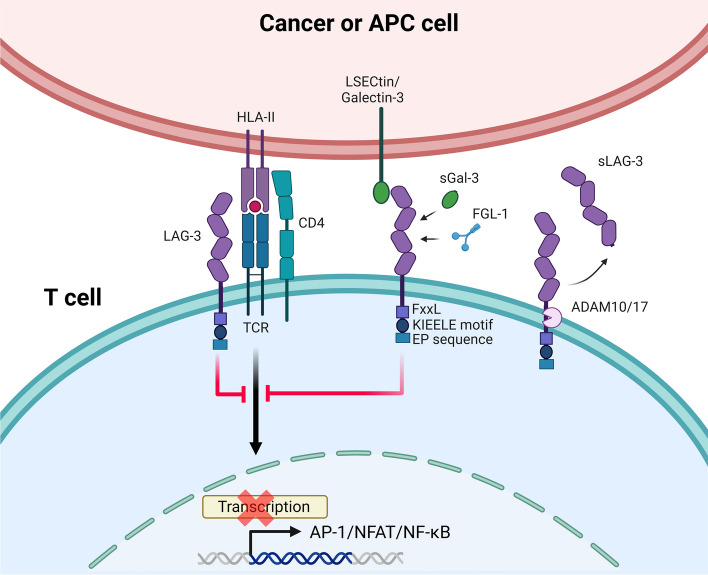
图2 LAG-3在免疫调节中的机制
● LAG3在肿瘤中的作用机制
①肿瘤微环境(TME)调控:LAG3通过结合MHCⅡ或FGL1,诱导CD8⁺T细胞耗竭,促进调节性T细胞(Treg)和M2型巨噬细胞浸润,构建免疫抑制性微环境,促进肿瘤免疫逃逸。此外,LAG3还可通过抑制CD8⁺T细胞功能,间接促进肿瘤细胞上皮-间质转化(EMT)相关信号通路(如TGF-β)活化,如在结直肠癌中FSTL1-LAG3轴与EMT正相关。阻断LAG3可恢复T细胞增殖和细胞毒性。
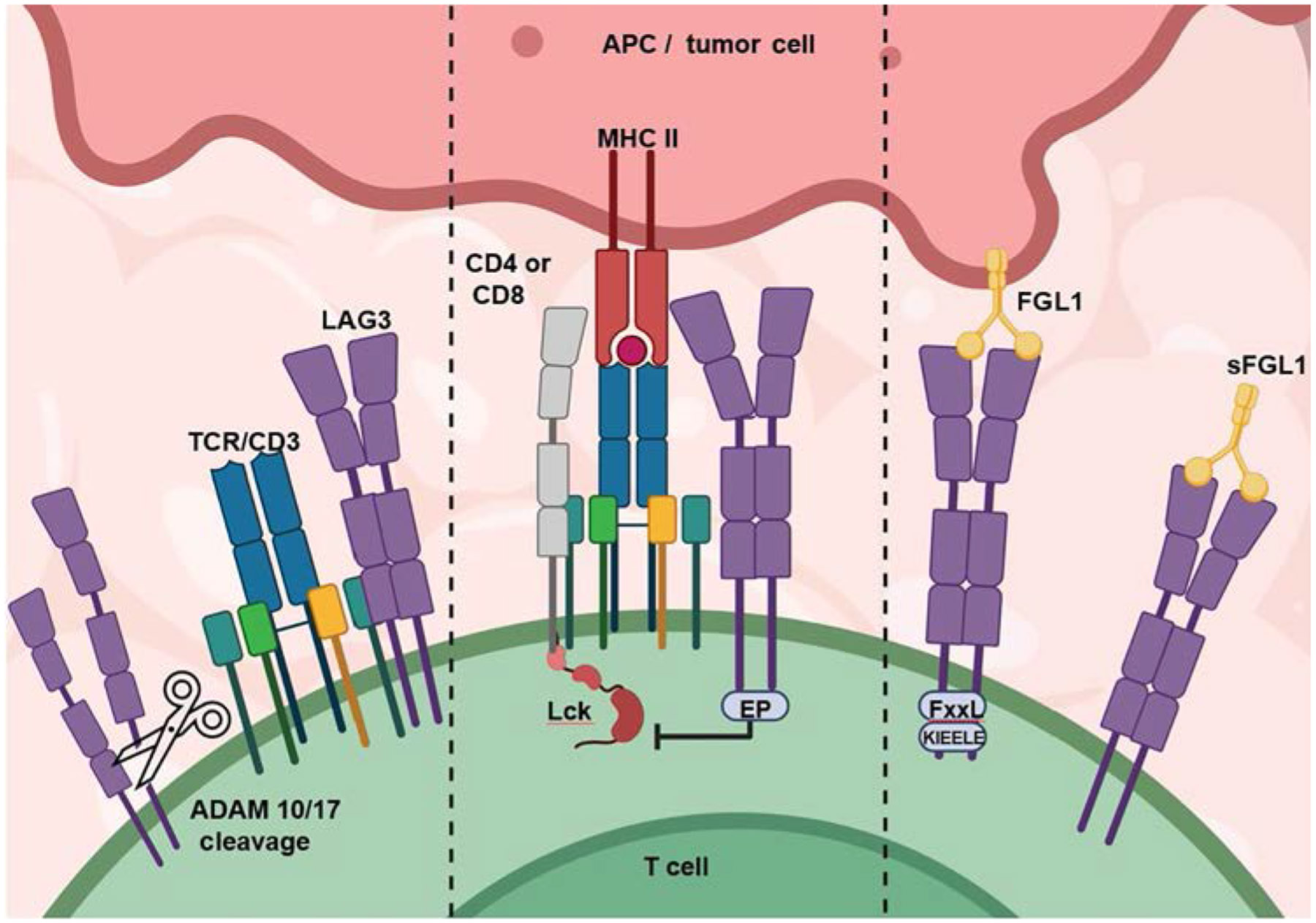
图3 LAG3在肿瘤微环境(TME)中的作用
②免疫逃逸协同作用:FGL1/LAG3轴与PD-1/PD-L1轴存在协同抑制效应,共表达于多种肿瘤的耗竭T细胞,双重阻断可显著增强T细胞活化。在PD-1耐药肿瘤中,FGL1/LAG3轴成为主要免疫逃逸途径,单独阻断即可恢复抗肿瘤免疫。
● LAG3在自身免疫性疾病的作用机制:LAG-3作为负调控因子,限制T细胞的增殖和免疫功能,防止其攻击正常组织。LAG-3缺陷导致T细胞增殖失控,加速自身免疫病(如1型糖尿病、心肌炎)进展。Tregs中LAG-3表达受IL-27调控,通过结合MHCII抑制DC成熟,维持免疫耐受。类风湿关节炎、多发性硬化等患者血清sLAG-3水平与疾病活动度正相关,可作为预后标志物。激动剂抗体(如IMP-761)通过激活LAG-3抑制T细胞功能,缓解炎症模型症状。
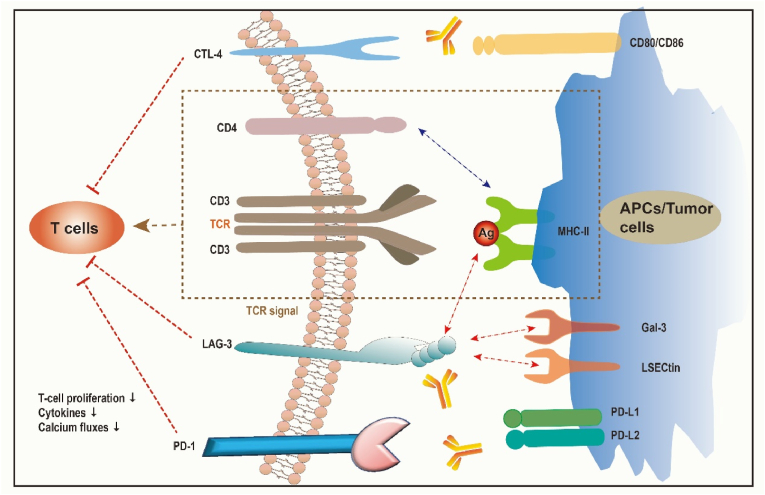
图4 LAG-3在自身免疫性疾病中的功能和机制
● LAG-3作为预后生物标志物的双重性
①阳性预后关联:在三阴性乳腺癌(TNBC)、胃癌、结直肠癌中,高LAG-3+TILs与更长的无转移生存期(MFS)和总生存期(OS)相关,可能反映活化T细胞的持续抗肿瘤效应。
②阴性预后关联:在肝细胞癌(HCC)、卵巢癌、黑色素瘤中,高LAG-3表达与肿瘤进展、耐药及不良预后相关,可能与T细胞过度耗竭有关。
三、LAG3靶向治疗的临床进展
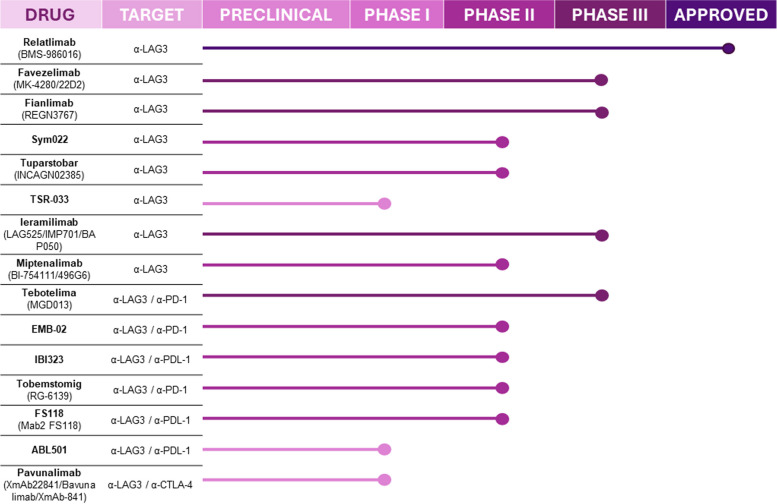
图5 LAG-3靶向治疗癌症的临床进展
● 靶向LAG3的单克隆抗体
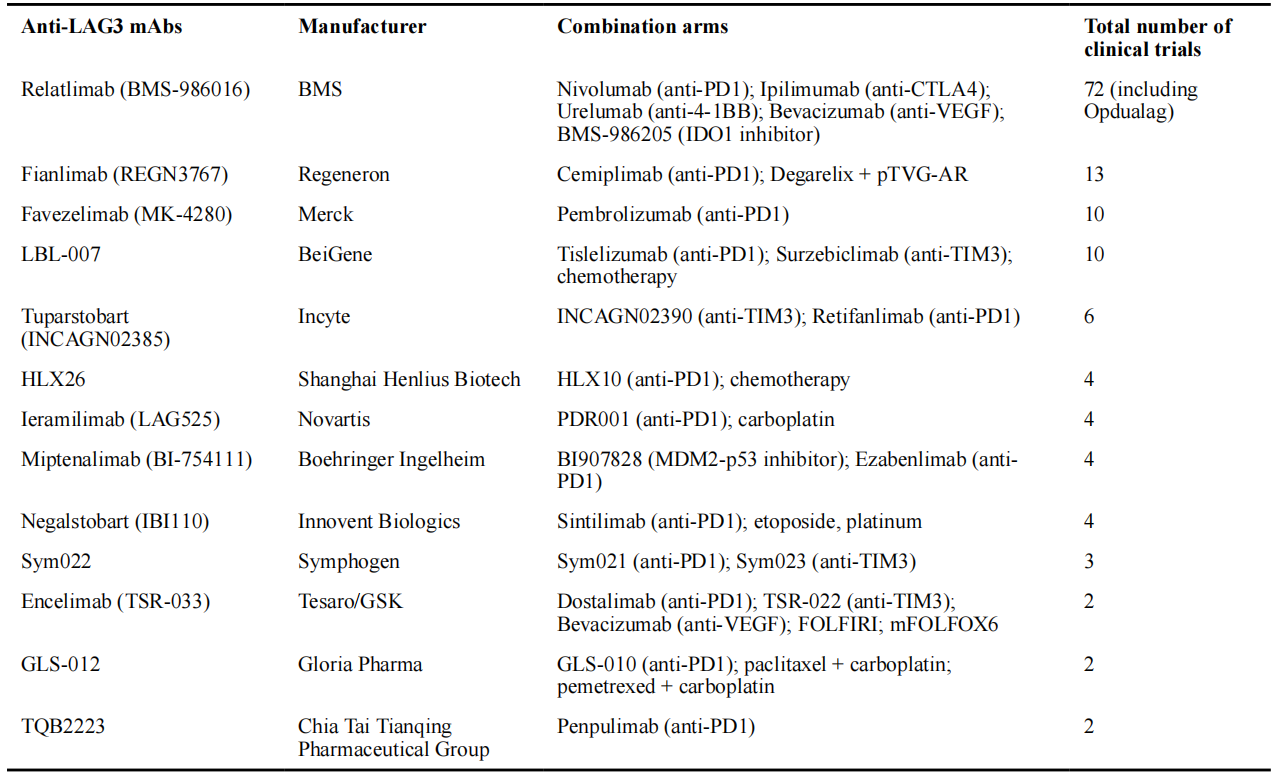
表1 用于治疗癌症的临床试验中靶向LAG3的单克隆抗体
● 靶向LAG3的单特异性抗体联合疗法
①Relatlimab(抗LAG3单抗)+Nivolumab(抗PD-1单抗):已获批用于晚期黑色素瘤,且在结直肠癌、膀胱癌的III期试验中均显示生存获益。相比Nivolumab单药显著延长中位无进展生存期(PFS),且安全性良好。目前正在开展Relatlimab联合Nivolumab治疗CLL、FL、HL的I/II期临床试验。
②Fianlimab(抗LAG3单抗)+Cemiplimab(抗PD-1单抗):I期试验中客观缓解率(ORR)达61.2%,但3级以上不良事件(AE)发生率为44%,主要为肾上腺功能不全。目前III期试验正在评估其在黑色素瘤和NSCLC中的疗效。
③Favezelimab(抗LAG3单抗)+Pembrolizumab(抗PD-1单抗):用于复发/难治性霍奇金淋巴瘤(R/RcHL)的II期试验显示,ORR达31%,12个月PFS率39%,对PD-1治疗失败患者仍有效。III期试验中,探索用于结直肠癌和霍奇金淋巴瘤的治疗。
④其他组合:LAG3mAb与CTLA4、TIM3、VEGF等靶点联合疗法正在临床试验中,但其中部分因疗效不足终止。
● 双特异性抗体(BsAbs)
1)靶向免疫细胞表面多重IRs:如Tebotelimab(LAG3/PD1)、Tobemstomig(LAG3/PD1),选择性结合PD1+LAG3+耗竭T细胞,降低脱靶毒性。
①Tebotelimab(MGD013):靶向LAG3/PD1的四价BsAb,I期试验显示单药ORR为19.4%,但irAEs发生率较高(68.4%),用于弥漫大B细胞淋巴瘤(DLBCL)的I期试验以及联合抗HER2抗体Margetuximab用于胃癌的II/III期试验正在进行。
②Tobemstomig(RO7247669):优先结合PD1的LAG3/PD1-BsAb,单药ORR为17.1%,联合化疗或TIGIT抑制剂的试验正在开展。
③Pavunalimab(XmAb22841):靶向LAG3/CTLA4的BsAb,与XmAb23104(PD-1/ICOSBsAb)联用的I期试验显示不良事件发生率低(20–24%),安全性优于传统联合疗法。
2)促进细胞间相互作用:
①FS118、ABL501、IBI323:靶向LAG3/PDL1的BsAb,通过桥接T细胞与肿瘤细胞或抗原呈递细胞(APCs)增强T细胞活化和抗肿瘤免疫。FS118的I期试验显示疾病控制率为54.8%,且毒性较低。
②GB266T:三特异性抗体(PDL1/TIGIT/LAG3),保留Fc功能以增强APCs与T细胞的相互作用,临床前模型中显示强效抗肿瘤活性。
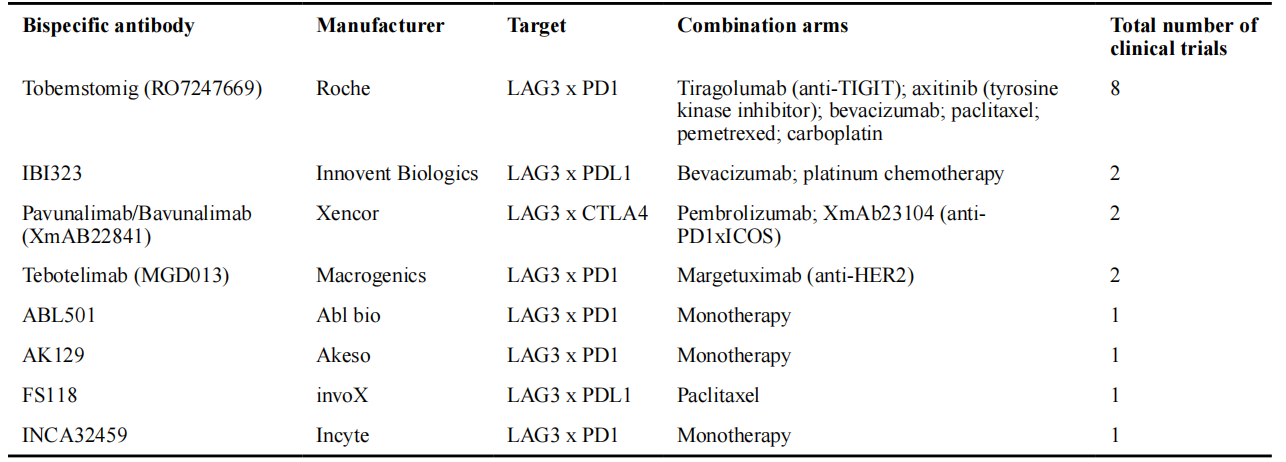
表2 用于治疗癌症的临床试验中靶向LAG3的双特异性抗体
● 其他新型疗法
①Eftilagimod-alpha(IMP321):可溶性LAG-3Ig融合蛋白,通过结合DCs表面MHCII,促进DC成熟及CD8+T细胞活化,III期试验评估其与紫杉醇联用在转移性乳腺癌中的疗效。与Pembrolizumab联用在黑色素瘤中ORR达50%,并可增强化疗疗效。
②纳米药物:纳米载体共递送siFGL1和siPD-L1可下调肿瘤微环境中免疫检查点表达,增强T细胞浸润。
③疫苗:双靶点疫苗(如FGL1/CAIXDNA疫苗)通过激活树突状细胞(DC),增强CD8+T细胞对肾癌的免疫应答。
④小分子抑制剂:靶向LAG-3与MHC-II/FGL1结合的小分子药物进入临床前研究,具口服生物利用度和肿瘤穿透性优势,处于早期研发阶段。如GSK-3抑制剂通过下调LAG-3转录增强免疫应答,可探索其与LAG-3单抗的协同效应。
● 联合治疗策略
1)与其他免疫检查点抑制剂联用:LAG3与TIM3、TIGIT等共阻断可克服PD-1耐药,如在肺癌模型中联合阻断LAG3和TIGIT显著抑制肿瘤生长,在AML模型中LAG-3与TIM-3双阻断可协同恢复T细胞功能。
2)与靶向治疗联用:
①LAG3抑制剂:可逆转EGFR-TKI耐药,如在NSCLC中联合Gefitinib增强抗肿瘤效应。
②PI3Kδ抑制剂:LAG-3阻断可增强PI3Kδ抑制剂的抗肿瘤效应,机制与减少Treg抑制和促进CD8+T细胞活化相关。
③GSK-3抑制剂:SB415286+抗LAG-3在B16黑色素瘤模型中诱导完全肿瘤消退,与CD8+T细胞增殖和细胞因子分泌增加相关。
3)与放化疗联用:
①化疗增敏:部分血液肿瘤对单一LAG-3阻断响应有限,需结合化疗(如阿扎胞苷)或表观调控药物(如HDAC抑制剂)逆转免疫抑制微环境。Tebotelimab与化疗(如卡培他滨+奥沙利铂)联用在HER2+胃癌的II/III期试验中显示初步疗效。
②放疗协同:微波消融或纳米粒子放疗联合LAG-3阻断可增强CD8+T细胞浸润,在MC38结直肠癌模型中显著抑制肿瘤生长。
4)与中药及细胞疗法联用:氧化苦参碱通过下调IL-6/STAT3通路降低FGL1表达,增强LAG3免疫治疗效果;CAR-T细胞联合LAG3抗体可增强对TNBC的杀伤作用。
5)与过继细胞疗法联用
①CAR-T细胞疗法:LAG-3抗体增强CD4+T细胞和双阴性T细胞(CD4-CD8-TC)的细胞毒性,在乳腺癌模型中上调T-bet和穿孔素表达。临床前研究显示,LAG-3抗体可增强CAR-T细胞对CLL的杀伤作用,相关临床试验待开展。
②肿瘤浸润淋巴细胞(TILs):LAG-3阻断联合TILs疗法在黑色素瘤中显示增强的持久应答。
四、LAG3在不同疾病中的病理机制
● 实体瘤应用:
1)黑色素瘤:LAG-3表达水平与黑色素瘤的进展、耐药相关。LAG-3在TILs表面高表达,可诱导T细胞耗竭,同时增强Tregs的免疫抑制功能,促进肿瘤免疫逃逸。此外还能协同PD-1通路促进免疫耐受。双重阻断可逆转T细胞功能失调,增强抗肿瘤免疫应答,显著延长无进展生存期(PFS)和总生存期(OS),且毒性低于CTLA-4/PD-1联合方案。
2)肾细胞癌(RCC):LAG-3与PD-1在肿瘤微环境中协同表达,抑制CD8+T细胞和NK细胞功能,且LAG-3表达水平与患者预后呈负相关。单药LAG-3抑制剂疗效有限,联合PD-1抑制剂在初治患者中客观缓解率(ORR)达30%,但对PD-(L)1经治患者响应不足(ORR7%)。配体FGL-1可能通过LAG-3介导免疫逃逸,但其独立作用机制仍存争议。
3)非小细胞肺癌(NSCLC):在NSCLC中,LAG3与PD-L1共表达患者接受抗PD-1治疗后,临床获益率和长期生存率更高,可作为独立预后因子。对PD-1抑制剂耐药的肿瘤常上调LAG-3,通过抑制T细胞代谢(如糖酵解)和DC成熟维持免疫抑制。relatlimab+nivolumab联合化疗在PD-L1≥1%亚组中显示ORR提升趋势(51.3%vs.43.7%),但整体未达显著差异。新辅助治疗中,relatlimab+nivolumab可诱导病理缓解(MPR30%),安全性与单药相当。
4)结直肠癌(CRC):
①微卫星不稳定型(MSI-H/dMMR):LAG-3抑制剂联合PD-1抑制剂在新辅助治疗中显示高病理缓解率(92%),可能与肿瘤免疫原性高相关。
②微卫星稳定型(MSS):LAG-3靶向治疗单药疗效有限,需结合其他通路(如Wnt/β-catenin)异常筛选患者。
5)胃癌/胃食管交界癌(GC/GEJC):LAG-3+Tregs在肿瘤微环境中富集,抑制效应T细胞浸润,联合化疗未能显著提升ORR(48%vs.61%),提示需更精准的生物标志物指导治疗。
6)肝癌(HCC):LAG-3与PD-L1在肝细胞癌中共表达,通过抑制CD8+T细胞和NK细胞功能促进肿瘤生长。relatlimab+nivolumab在TKI经治患者中疾病控制率(DCR)达60%,双特异性抗体Tebotelimab单药ORR17.1%,显示初步活性但需更大样本验证。
7)三阴性乳腺癌(TNBC):LAG-3抑制CD8+T细胞浸润和细胞毒性,与Gal-3协同促进肿瘤进展。Ieramilimab+spartalizumab在初治患者中ORR26.3%,但经治患者仅5.3%,提示早期干预可能更有效。
8)其他肿瘤:LAG3的表达还与膀胱癌、子宫内膜癌等的免疫细胞浸润密度和预后相关,如肌层浸润性膀胱癌中LAG3⁺T细胞浸润与化疗耐药和不良生存独立相关。
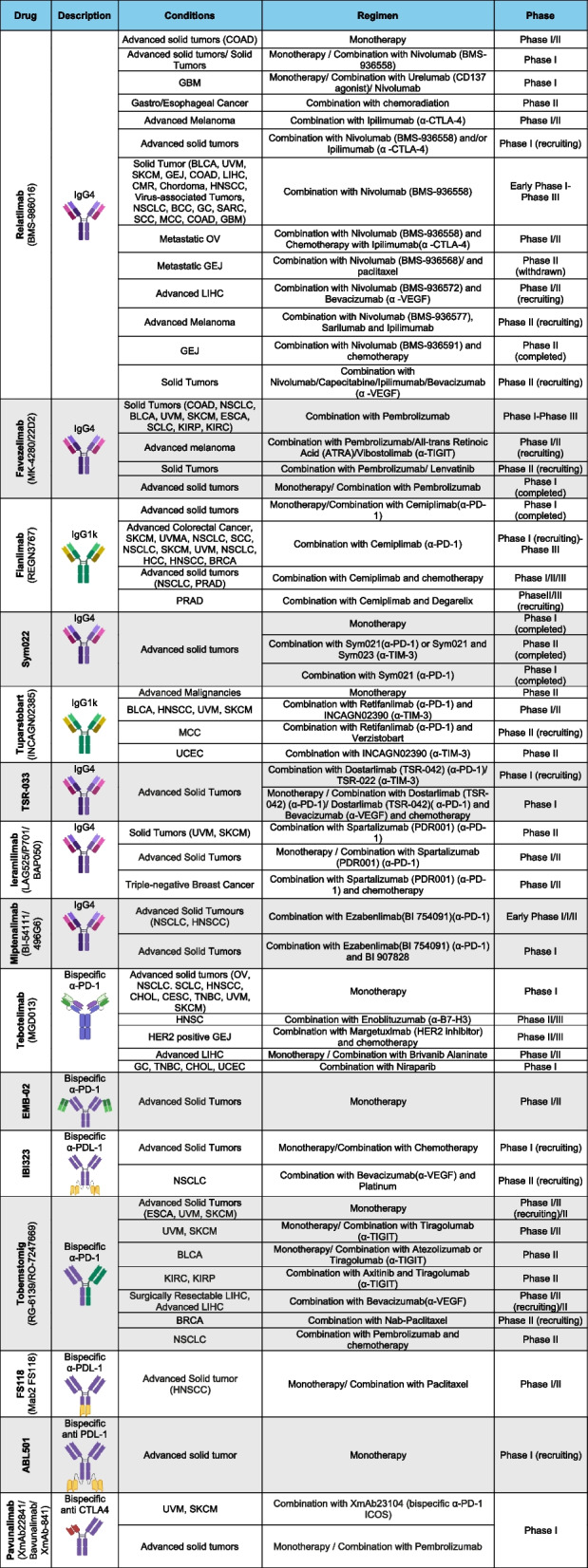
表3 靶向LAG-3治疗实体瘤的临床试验
● 血液肿瘤应用:在慢性淋巴细胞白血病(CLL)、霍奇金淋巴瘤中,LAG-3高表达与不良预后相关,联合PD-1阻断可恢复T细胞抗肿瘤活性。
1)慢性淋巴细胞白血病(CLL):CLL患者的白血病细胞及血清中sLAG-3水平显著升高,与疾病进展和不良预后相关。在CLL的临床前模型中,阻断LAG-3可恢复T细胞对白血病细胞的杀伤能力,联合PD-1抑制剂进一步增强疗效。
2)霍奇金淋巴瘤(HL):HL患者的肿瘤浸润T细胞(TILs)中LAG-3高表达,与PD-1共表达于耗竭CD8⁺T细胞,抑制抗原特异性免疫应答。LAG-3⁺CD4⁺T细胞的存在与HL患者的肿瘤进展相关,清除此类细胞可增强CD8⁺T细胞的抗肿瘤效应。
3)急性髓系白血病(AML):AML患者骨髓中LAG-3⁺PD-1⁺CD8⁺T细胞比例显著高于健康人群,提示T细胞功能耗竭。
4)滤泡淋巴瘤(FL):LAG-3表达于肿瘤浸润T细胞,与PD-1共表达时预示患者预后不良,且与肿瘤微环境中免疫抑制性细胞因子(如IL-10)水平升高相关。
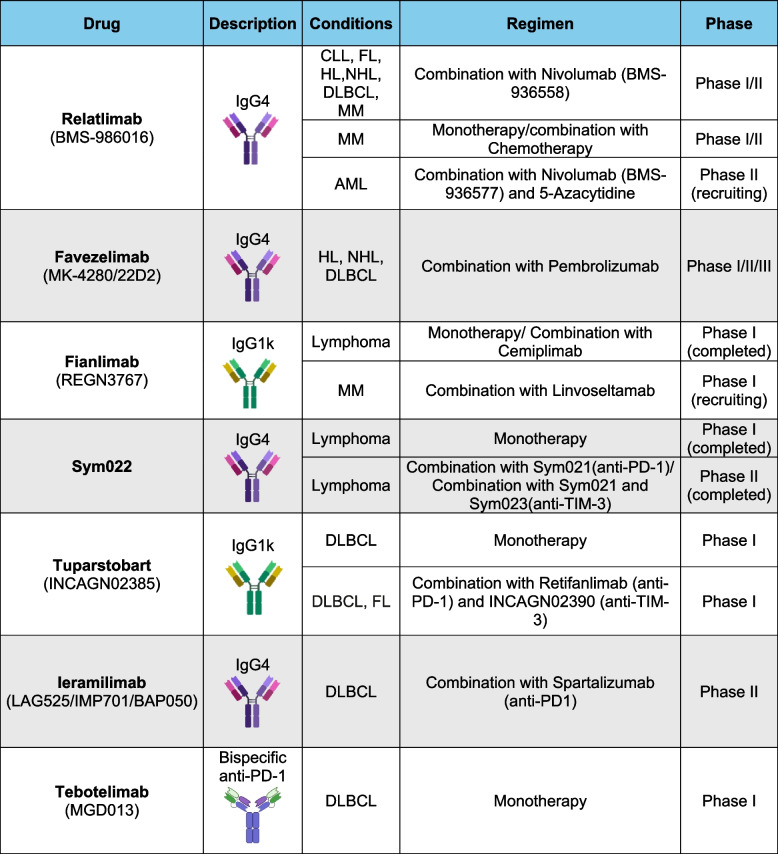
表4 血液系统癌症中靶向LAG-3的临床试验
● 自身免疫疾病应用
1)系统性红斑狼疮(SLE):SLE患者Tregs表面LAG-3表达降低,导致其抑制效应T细胞的能力减弱,无法有效控制自身免疫反应。SLE患者中LAG-3在Tregs和效应T细胞表面高表达,与疾病活动度(SLEDAI评分)正相关,其血清浓度可反映炎症程度。并且血清sLAG-3水平降低与SLE患者病情进展相关,可能成为预测疾病恶化的指标。LAG-3缺陷间接增强CD4+T细胞对B细胞的辅助功能,促进自身抗体(如抗dsDNA抗体)产生,加剧SLE模型中的肾小球炎症。
2)1型糖尿病(T1D):LAG-3通过维持CD8+T细胞的“restrained”表型(类似耗竭状态)抑制其攻击胰岛β细胞。在LAG-3缺陷小鼠中,CD8+T细胞的“restrained”表型消失,糖酵解代谢增强,加速T1D进展;而Tregs表面LAG-3缺失则无法有效抑制自身免疫反应。传统认为CD4+T细胞主导T1D,但LAG-3缺陷模型显示CD8+T细胞也可独立驱动疾病,提示LAG-3对两类T细胞均有调控作用。
3)类风湿关节炎(RA):RA患者中LAG-3+Tregs比例升高,但其分泌IL-10的能力下降,导致促炎因子(如TNF-α、IL-6)失衡。血清sLAG-3水平与疾病活动度(如关节肿胀程度)正相关,其主要来源于Tregs表面LAG-3的蛋白酶切割。靶向LAG-3可增强Tregs的抑制功能,减少关节炎症,如激动剂抗体IMP-761在动物模型中显示抗炎潜力。
4)多发性硬化(MS):MS患者外周血中LAG-3+T细胞数量减少,与中枢神经系统炎症加重相关;血清sLAG-3水平较高者预后较好,提示LAG-3可能抑制自身反应性T细胞向脑内浸润。LAG-3可能通过抑制Th1/Th17细胞分化,减少其分泌IFN-γ和IL-17,从而减轻神经髓鞘损伤。
5)炎症性肠病(IBD):LAG-3+T细胞在肠道黏膜中富集,其数量与内镜下炎症程度正相关。阻断LAG-3可激活效应T细胞,加重结肠炎;而维持LAG-3功能可抑制过度免疫反应。LAG-3通过抑制CD4+T细胞的糖酵解代谢,减少促炎细胞因子(如IL-17)分泌,维持肠道免疫稳态。
五、挑战与未来方向
● 机制研究的局限性
①配体复杂性:MHCII作为主要配体的作用已明确,但FGL1、LSECtin等配体的贡献仍需验证,且不同物种间存在差异(如小鼠vs.人类MHCII稳定性)。
②信号通路未知:缺乏LAG-3下游信号分子的明确研究,需通过蛋白质组学、CRISPR筛选等技术解析。
● 生物标志物开发:缺乏统一的生物标志物检测标准,目前LAG3表达水平、FGL1的预测价值有限,sFGL1和sLAG3的临床意义尚不明确,需探索LAG-3表达水平、T细胞耗竭状态(如PD-1共表达)及肿瘤微环境细胞组成(如Treg比例)的联合预测价值。
● 毒性管理与联合优化:尽管LAG-3抑制剂单药毒性较低,但与其他ICIs联用可能增加irAEs(如肾上腺功能不全),需探索剂量优化和个体化治疗策略。
● 新型药物设计:开发同时阻断LAG-3与多种配体(如MHCII/FGL1)的双特异性抗体,或小分子抑制剂靶向胞内信号基序。
● 联合治疗策略:探索LAG-3抑制剂与放疗、表观药物或多靶点阻断(如TIM-3、TIGIT)的协同效应,以克服耐药性。