一、IL-17的基本生物学特性
● IL-17家族成员:IL-17家族包含6个成员(IL-17A至IL-17F),其中IL-17A与IL-17F同源性最高(超50%),可形成异源二聚体发挥作用,是Th17细胞的主要效应因子。其他成员多以同源二聚体形式存在。各成员均为分泌型糖蛋白,依赖保守的半胱氨酸结折叠结构与特异性受体结合发挥功能。
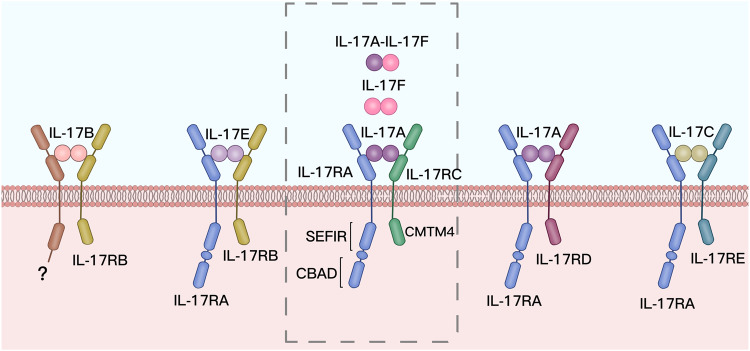
图1 IL-17细胞因子和受体家族结构示意图
● IL-17受体家族:IL-17受体家族(IL-17RA-RE)均为单次跨膜蛋白,胞外域含纤连蛋白Ⅱ型结构域,负责配体识别;胞内域含SEFIR结构域,通过招募衔接蛋白Act1激活下游通路传导信号。
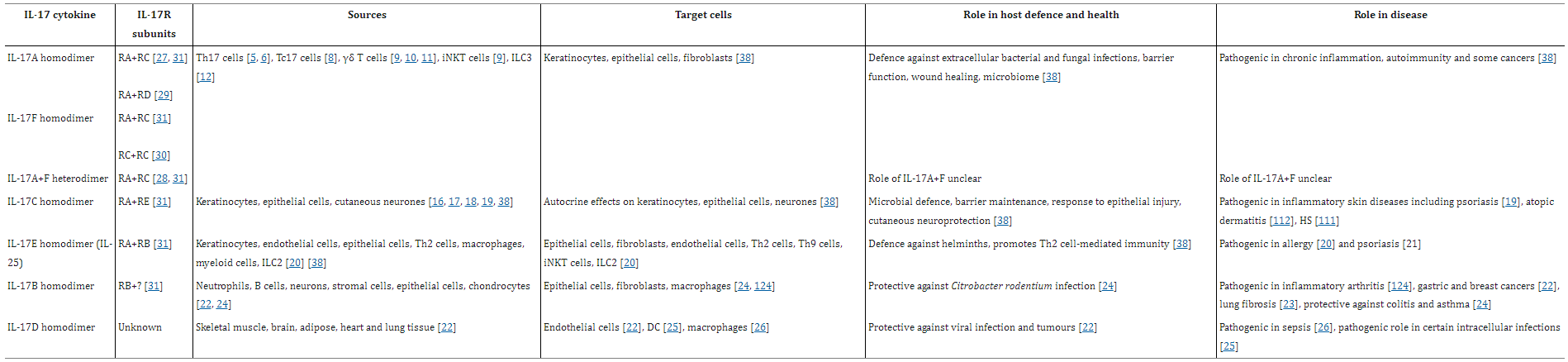
表1 IL-17细胞因子及其受体、细胞来源、靶细胞和功能
● 配体-受体配对:
①IL-17A/F:主要通过IL-17RA/IL-17RC异二聚体传递信号。
②IL-17B:结合IL-17RB,调控代谢和纤维化。
③IL-17C:与IL-17RA/IL-17RE结合,参与黏膜免疫。
④IL-17E(IL-25):通过IL-17RA/IL-17RB异二聚体激活2型免疫。
⑤IL-17D:结合IL-17RA/IL-17RD,功能尚不明确。
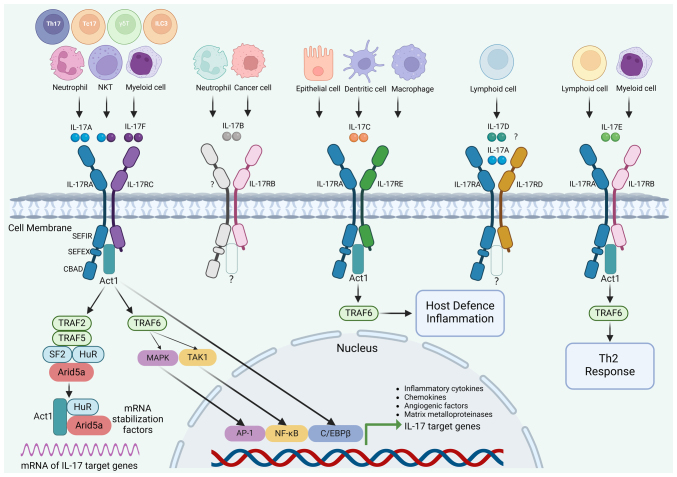
图2 IL-17家族成员和细胞内信号转导通路
二、IL-17的表达调控及信号传导
● IL-17细胞来源:IL-17主要由Th17、Tc17、γδT细胞、NK细胞等免疫细胞分泌,也可来自肿瘤相关成纤维细胞(CAFs)、髓系细胞和上皮细胞。
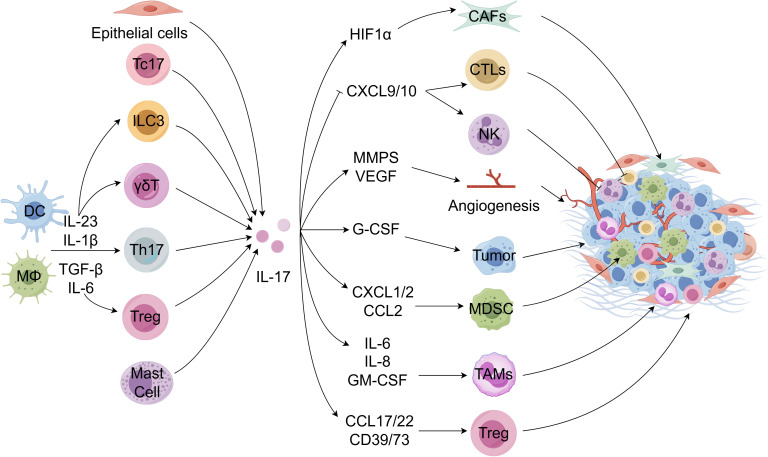
图3 TME中IL-17的细胞来源
● IL-17信号传导
①经典通路:IL-17配体与受体结合后,通过Act1-TRAF6-TAK1复合物激活NF-κB和MAPK(如ERK、JNK、p38)通路,诱导促炎因子(如TNF、IL-6、IL-8)、趋化因子(如CXCL1、CCL20)和基质金属蛋白酶(MMPs)等基因表达,驱动炎症反应。Act1通过结合HuR、ARID-5A稳定mRNA,或通过Regnase-1促进降解,动态调节炎症强度。
②非经典通路:部分成员(如IL-17E)可通过其他途径(如STAT3)发挥作用。
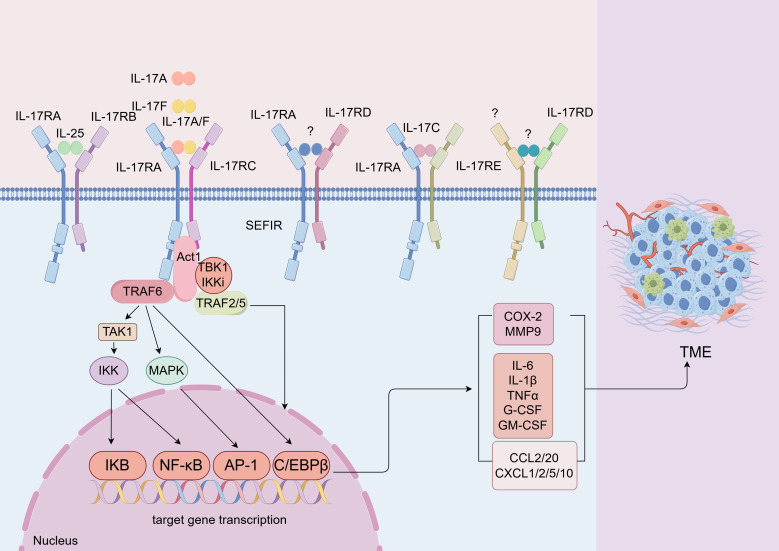
图4 IL-17信号转导
● IL-17协同信号通路
①与生长因子互作:IL-17与FGF2协同修复肠上皮损伤,通过Act1-GRAB2-SOS1-ERK1/2轴促进细胞增殖。
②代谢调控:IL-17诱导成纤维细胞表达肉碱棕榈酰转移酶1A(CPT1A),增强脂肪酸氧化,支持细胞增殖和炎症代谢需求。
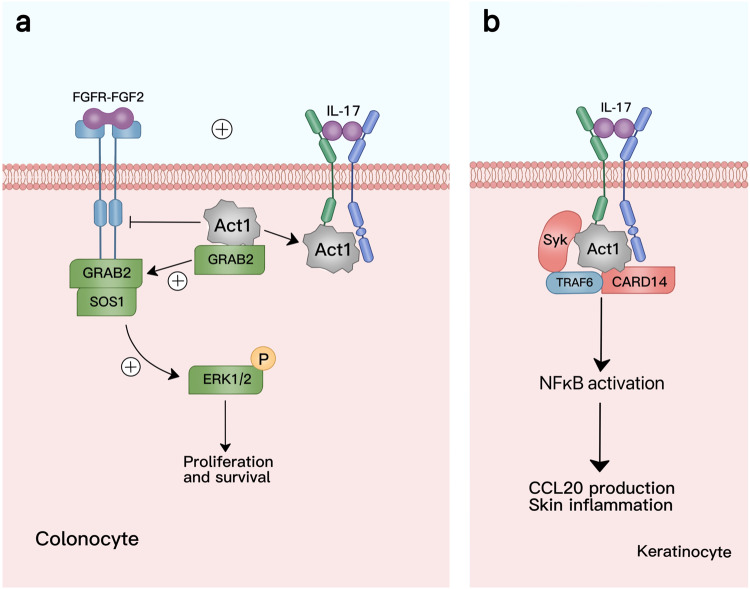
图5 IL-17调节的协同信号相互作用
三、IL-17的功能多样性
● IL-17生理功能
①宿主防御:在健康状态下,IL-17主要表达于肠道、皮肤等屏障组织,通过诱导中性粒细胞趋化,促进抗菌肽(如β-防御素)和趋化因子(如CXCL1)分泌,介导对细菌、真菌、病毒等病原体的免疫应答,增强皮肤屏障的抗菌能力,维持微生物稳态。
②组织修复:病原体突破屏障时,IL-17通过招募中性粒细胞,调节成纤维细胞和上皮细胞功能,参与伤口愈合和炎症消退,与FGF2、VEGF等协同促进上皮再生,维持黏膜屏障完整性,但过度表达可能延迟愈合。
③菌群-免疫互作:肠道菌群通过激活IL-1R/MyD88信号诱导IL-17+细胞,维持屏障完整性。菌群失调(如IL-17R缺陷小鼠的肠道菌群过度生长)可诱发系统性Th17活化,加剧自身免疫病。
● IL-17病理功能
1)自身免疫病中的促炎作用:IL-17A是银屑病、类风湿关节炎等疾病的关键驱动因子,通过诱导CXCL13和CCL19促进三级淋巴器官(TLO)形成,,协同TNF-α、IL-1β等增强促炎基因表达,维持慢性炎症。
2)促肿瘤作用
①肿瘤细胞增殖与转移:刺激肿瘤细胞增殖(如CRC中激活ERK/p38MAPK通路)、抑制凋亡、促进血管生成(如VEGF、CXCL1)和上皮-间质转化(EMT)。
②免疫抑制微环境:招募髓源性抑制细胞(MDSCs)、调节性T细胞(Tregs),抑制细胞毒性T细胞(CTLs)和NK细胞浸润。
③微生物调控:与肠道/肺部微生物互作,如分段丝状菌(SFB)通过诱导IL-17促进CRC,肠道菌群代谢物(如吲哚-3-乳酸)可抑制IL-17通路。
3)抗肿瘤作用
①免疫激活:在部分模型中招募CTLs和NK细胞(如卵巢癌中诱导CXCL9/10),增强抗肿瘤免疫。
②细胞毒性:通过ROS/NLRP3通路诱导肿瘤细胞焦亡(如CRC)。
四、IL-17的靶向治疗及临床进展
● 靶向治疗策略
①单克隆抗体:靶向IL-17A(如secukinumab)或IL-17RA(如brodalumab)已进入临床试验,可增强抗VEGF治疗效果。
②联合治疗:IL-17抑制剂与ICI(如抗PD-1)联用可逆转耐药,在黑色素瘤和CRC模型中显示协同效应。IL-17抑制剂与放疗/化疗联用可减轻放疗/化疗诱导的炎症毒性,增强放疗/化疗的敏感性。
③微生物干预:补充相关益生菌(如L.reutii)可抑制Th17细胞分化,减少IL-17分泌,在CRC模型中延缓肿瘤进展。粪菌移植(FMT)通过重塑肠道菌群平衡,减少促IL-17分泌的微生物(如SFB),可能增强IL-17抑制剂的疗效。
④双特异性抗体:同时靶向IL-17和PD-L1,实现免疫激活与抑制的协同调控。
⑤基因编辑:通过CRISPR-Cas9敲除肿瘤细胞IL-17R,增强其对CTLs的敏感性。
⑥新型制剂:开发组织特异性抑制剂或小分子药物,避免全身免疫抑制。
⑦疫苗疗法:DC疫苗联合放疗可诱导Th17免疫,延长小鼠生存期,但需解决肿瘤异质性问题。
⑧外泌体与新型疗法:外泌体搭载miR-451抑制剂可减少Th17分化,逆转免疫抑制;新型分子如Molecule6通过抑制IL-17伴侣蛋白,诱导肿瘤细胞凋亡。
● IL-17的诊断与预后价值
1)预测性标志物:肿瘤内Th17细胞密度、IL-17通路基因(如IL-17A、IL-17RA)表达水平健康人群有差异,可作为潜在预测标志物,用于筛选患者。
2)微生物标志物:肠道菌群中IL-17相关菌属(如拟杆菌属、肠球菌属)的丰度与IL-17A水平正相关,可用于疗效预测。调控共生菌可诱导保护性IL-17反应,减少自身免疫病风险。
3)预后矛盾性:
①不良预后:肿瘤内IL-17+细胞浸润与更短生存期相关,且与WHO分级正相关。
②潜在保护作用:部分研究显示IL-17与较长无进展生存期(PFS)相关,可能与激活NK细胞和CTLs有关。
4)治疗监测:放疗后IL-17水平下降可能提示疗效,但其作为复发预测标志物的价值需进一步验证。
● IL-17的疗效与毒性平衡
①炎症风险:过度抑制IL-17可能破坏黏膜屏障,增加感染风险(如真菌、细菌),需监控宿主防御功能。
②组织特异性效应:在放疗中,IL-17对正常组织(如骨髓)的保护作用可能限制其全身抑制的可行性,需开发局部递送技术
● IL-17介导的治疗抵抗机制
1)化疗耐药
①代谢重编程:IL-17A通过诱导铜代谢基因STEAP4表达,增强结直肠癌(CRC)对5-FU的耐药性,减少化疗诱导的细胞凋亡。
②药物外排与应激适应:在乳腺癌中,IL-17通过激活ERK/HER1通路,增强肿瘤细胞对酪氨酸激酶抑制剂和多西他赛的抵抗。
2)放疗毒性与抵抗
①炎症加剧:IL-17A加剧放疗诱导的肺纤维化和肺炎(如放射性肺损伤RILI),通过NF-κB通路激活成纤维细胞和免疫细胞,释放促纤维化因子(如TGF-β)。
②免疫抑制微环境:放疗后IL-17A招募MDSCs和Tregs,抑制CD8+T细胞功能,削弱放疗的免疫原性celldeath效应。
3)免疫检查点治疗(ICI)耐药
①PD-L1上调:IL-17A通过p65/NRF1/miR-15b-5p轴或ROS/Nrf2/p62通路,增加肿瘤细胞PD-L1表达,抑制T细胞活化(如NSCLC、CRC)。
②免疫细胞耗竭:在黑色素瘤和肺癌中,IL-17A诱导CD8+T细胞耗竭(如高表达PD-1、TIM-3),并招募MDSCs形成“免疫沙漠”微环境。
③微生物协同耐药:肠道微生物失调(如具核梭杆菌)通过增强IL-17信号,削弱抗PD-1治疗在CRC中的疗效。
五、IL-17在不同疾病中的具体作用
● 癌症:
①结直肠癌(CRC):在CRC中,IL-17在早期可促进结肠上皮细胞增殖、抑制肿瘤细胞分泌CXCL9/10以减少免疫细胞浸润;进展期能招募免疫抑制细胞、促进血管生成和基质重塑,并与肠道微生物协同促癌。此外,IL-17A还可通过STEAP4介导化疗耐药。但IL-17F通过维持肠上皮屏障发挥抗肿瘤作用,部分模型中IL-17A还可通过ROS/NLRP3通路诱导肿瘤细胞焦亡并招募CD8+T细胞发挥抗肿瘤效应。
②乳腺癌:IL-17在乳腺癌中以促肿瘤为主,IL-17A能通过相关信号通路促进肿瘤细胞增殖、转移和化疗耐药,诱导乳腺癌细胞上皮-间质转化(EMT)增强干性和转移能力,还可激活免疫抑制细胞。IL-17B通过激活ERK/β-catenin通路加速肿瘤进展。但IL-17E在部分细胞系中有诱导癌细胞凋亡的抗肿瘤效果。
③非小细胞肺癌(NSCLC):IL-17在NSCLC中主要表现为促肿瘤效应,IL-17A可激活多条信号通路促进肿瘤细胞增殖、EMT、干性维持和免疫逃逸,还能诱导免疫抑制细胞浸润,介导免疫检查点治疗耐药。但在特定模型下,IL-17可激活STAT1通路增强抗肿瘤免疫。
④肝癌(HCC):IL-17在HCC中以促肿瘤为主,IL-17A促进肝祖细胞向癌症干细胞转化、加速肿瘤代谢重编程、招募免疫抑制细胞和促进血管生成,增强肿瘤细胞侵袭转移能力。但IL-17F可通过抑制血管内皮细胞增殖及VEGF分泌延缓肿瘤生长。
⑤胃癌(GC):IL-17在GC中以促肿瘤为主,IL-17A通过激活相关通路驱动细胞增殖、促进EMT和肿瘤干细胞活化,还能诱导免疫抑制细胞浸润和促进血管生成,整体促进GC进展与转移。
⑥胰腺癌(PDAC):IL-17在PDAC中以促肿瘤为主,IL-17A诱导中性粒细胞胞外陷阱形成介导免疫治疗耐药、增强肿瘤细胞干性,且肠道微生物可通过调控IL-17信号影响癌细胞氧化应激适应性。此外,IL-17B通过激活ERK1/2通路,诱导趋化因子分泌并招募免疫抑制性细胞,协同重塑微环境,加速PDAC侵袭与代谢异常,整体形成依赖IL-17的促癌网络。
⑦卵巢癌(OC):IL-17在OC中以促肿瘤为主,IL-17A促进癌症干细胞自我更新、抑制免疫细胞浸润和上调免疫逃逸相关分子。但在部分模型中,IL-17能招募免疫细胞发挥抗肿瘤作用。
⑧食管癌(ESCC):IL-17在ESCC中的作用机制呈现双向性,IL-17A可促进细胞侵袭转移,并抑制抗肿瘤免疫;但肿瘤浸润的IL-17+肥大细胞能招募免疫细胞增强抗肿瘤免疫,且IL-17还可诱导中性粒细胞杀伤肿瘤细胞,形成“促炎-抗肿瘤”的复杂平衡,其净效应取决于微环境中免疫细胞的组成与功能状态。
⑨黑色素瘤:IL-17在黑色素瘤中的作用机制具有复杂性,IL-17A促进肿瘤细胞增殖、诱导免疫逃逸和T细胞耗竭,但在BRAFV600突变型黑色素瘤中,IL-17可增强免疫细胞活性,协同免疫治疗,显示出抗肿瘤潜力。
● 自身免疫疾病:
①银屑病/关节炎:Th17细胞分泌的IL-17A/F驱动角质形成细胞增殖和炎症因子释放,导致皮肤角化过度和关节侵蚀,靶向IL-17A的secukinumab等药物已获批治疗。IL-17E(IL-25)通过STAT3通路加剧皮肤炎症,其抑制剂可缓解模型小鼠症状。
②炎症性肠病(IBD,如克罗恩病、溃疡性结肠炎):IL-17A促进肠道炎症和黏膜损伤,但过度抑制可破坏屏障功能,诱发机会性感染(如念珠菌)。IL-17F通过调节菌群诱导Treg细胞,抑制结肠炎相关癌变。临床试验显示,secukinumab和brodalumab用于克罗恩病时可能加重症状,提示需谨慎平衡炎症抑制与屏障保护。
③强直性脊柱炎(AS):IL-17A通过JAK2/STAT3通路激活成骨细胞,促进新骨形成和关节侵蚀,血清IL-17A水平与疾病活动度正相关。secukinumab和ixekizumab显著改善脊柱炎症和放射学进展,减少新骨形成。
④类风湿关节炎(RA):IL-17A诱导滑膜成纤维细胞分泌MMPs和趋化因子,促进关节破坏;γδT17细胞在模型中加剧关节炎进展。尽管IL-17抑制剂在动物模型中有效,但临床试验对RA疗效有限,可能与Th17细胞异质性及Ex-Th17细胞主导炎症有关。
⑤系统性红斑狼疮(SLE):IL-17A促进浆细胞存活(通过p38通路稳定Bcl-xLmRNA),增加抗双链DNA抗体产生,加重肾脏损伤。Th17/Treg失衡(Th17增多、Treg减少)驱动自身抗体生成和免疫复合物沉积,IL-23/IL-17轴参与疾病恶化。靶向IL-23(如ustekinumab)间接抑制Th17分化,显示潜在疗效,但直接靶向IL-17的临床试验尚在早期。
⑥多发性硬化(MS):IL-17A促进Th17细胞穿越血脑屏障,加剧神经炎症,在实验性自身免疫性脑脊髓炎(EAE)模型中加重症状。secukinumab减少MS患者脑病灶,但未显著改善长期预后,可能与炎症机制多样性有关。
⑦自身免疫性葡萄膜炎:IL-17A加剧视网膜炎症和血-眼屏障破坏,但部分模型中显示抗炎作用,机制尚不明确。
⑧1型糖尿病:Th17细胞浸润胰腺,IL-17A诱导β细胞凋亡,抗IL-17治疗可延缓NOD小鼠糖尿病进展。
⑨化脓性汗腺炎(HS):IL-17在HS中发挥关键作用。在HS患者中,毛囊阻塞后,其内容物释放激活炎症免疫通路,促进Th17细胞产生IL-17A和IL-17F,招募中性粒细胞等免疫细胞,形成炎症反馈循环,加重炎症。
● IL-17在不同类型的感染中的作用
①细菌感染:通过诱导抗菌肽(如hBD-2、S100A8/A9)和趋化因子(CXCL2、GM-CSF)招募中性粒细胞,增强宿主防御。例如,γδT细胞和Th17细胞在金黄色葡萄球菌感染中分泌IL-17,控制细菌负荷并促进伤口愈合,但铜绿假单胞菌感染中IL-17的作用存在矛盾,可能与iNKT细胞等来源相关。
②真菌感染:驱动Th17和γδT17细胞应答,抑制真菌增殖。白色念珠菌感染时,Th17细胞和ILC3s产生IL-17,协同IL-17F清除病原体;马拉色菌等共生菌在屏障受损时,通过IL-17诱发过度炎症,加剧特应性皮炎等病理。
③寄生虫感染:在利什曼原虫感染中,IL-17加剧皮肤炎症,与共生菌(如表皮葡萄球菌)协同扩大病变,但γδT17细胞在部分模型中显示保护作用;疥螨感染中,IL-17+T细胞浸润与病情严重程度相关。
④病毒感染:作用机制尚不明确,人类乳头瘤病毒(HPV)感染患者血清IL-17水平降低,可能与感染易感性相关,但IL-17抑制剂治疗银屑病时可能诱发病毒相关皮疹,提示其免疫调节的复杂性。